3.7
Kontrola kvality laboratorního vyšetření
Zajištění analytické spolehlivosti laboratorních vyšetření patří k základním povinnostem každé laboratoře. Z velké části je jí dosaženo prováděním kontroly kvality. Podstatnou část kontroly kvality představuje provádění analýz kontrolních vzorků, jejich správné zhodnocení a v případě potřeby včasná reakce laboratoře na zjištěné závady.
Podle toho, zda je kontrola prováděna samotnými pracovníky laboratoře či nezávislým kontrolním orgánem, rozlišujeme interní kontrolu kvality a externí hodnocení kvality.
3.7.1
Vnitřní kontrola kvality
Vnitřní kontrola kvality (Internal Quality Control, IQC) je prováděna pracovníky laboratoře; kontrolována je preciznost i pravdivost analýz. Vnitřní kontrola kvality se provádí formou speciálních počítačových programů, které patří k programovému vybavení analyzátorů a jsou i nedílnou součástí laboratorních informačních systémů.
S každou sérií stanovení se provádí analýza kontrolního vzorku. Hodnoty kontrolních vzorků by měly respektovat klinickou potřebu (např. blízko rozhodovací meze), často se doporučuje užívat kontrolní vzorky na více hladinách (normální, snížené a zvýšené hodnoty). Protože užíváme stále stejný kontrolní vzorek, musí se změřené hodnoty co nejméně lišit od dlouhodobého průměru. Výhodné je grafické znázornění výsledků (tzv. regulační graf). Body zde znamenají výsledky jednotlivých kontrolních analýz a v ideálním případě by se měly pohybovat v rozmezí x̄ ± 2s, zjištěném v předcházejícím období. Obvykle se užívají komerčně vyráběná kontrolní séra se známou cílovou koncentrací a s udaným rozmezím, v kterém se má měřená koncentrace pohybovat; regulační graf pak vedle kontroly preciznosti umožňuje realizovat současně i kontrolu pravdivosti; v jeho středu se místo průměrné hodnoty x̄ nachází cílová hodnota x0.
+
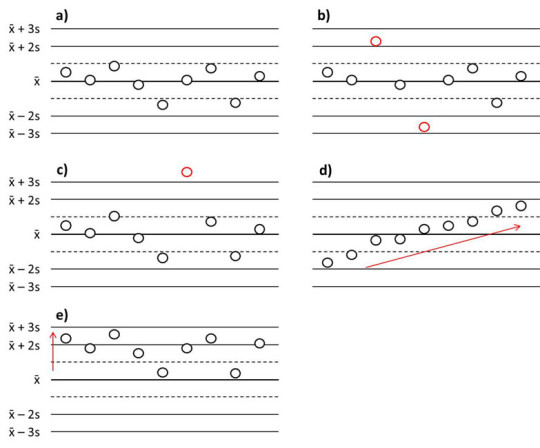
Regulační diagram – metoda je pod kontrolou, jestliže mimo rozmezí x̄ ± 2s leží maximálně 5 % výsledků kontrolních vzorků (a); v případě, že mimo toto rozmezí je větší podíl výsledků (b), leží-li i jen jeden výsledek mimo rozmezí x̄ ± 3s (c), narůstá-li (klesá-li) plynule jejich hodnota (d) či jsou-li všechny výsledky odchýleny jedním směrem (e), je nutné prověřit kvalitu metody
Jinou metodou kontroly pravdivosti metody je dlouhodobé sledování průměrných hodnot analyzovaných vzorků. Aritmetický průměr se nepočítá ze všech výsledků, ale jen z těch, které jsou uvnitř referenčních mezí („average of normals“). Někdy se užívají meze poněkud širší, než které určují referenční rozmezí, v žádném případě však do výpočtu nesmějí být zahrnuty extrémní výsledky. Takto spočítaný denní průměr výsledků se pohybuje v poměrně úzkém rozmezí a citlivě reaguje na systematickou chybu metody.
3.7.2
Externí hodnocení kvality
Externí hodnocení kvality (EHK – External Quality Assessment, EQA) je založené na porovnání výsledků dosažených v laboratoři s výsledky dosaženými v laboratořích ostatních. Organizuje ho pověřená instituce, v České republice je to Systém externí kontroly kvality (SEKK). Cílem je zlepšení analytické činnosti, projevující se dosažením maximální shody výsledků měření stejných vzorků (a tedy i vzorků pacientů) v různých laboratořích; hovoříme pak o mezilaboratorní srovnatelnosti.
K zásadám externího hodnocení kvality patří obvykle užití dvou kontrolních vzorků (jeden s fyziologickou, druhý s patologickou hodnotou koncentrace analyzované látky). Jak již bylo uvedeno, hodnotí se míra shody výsledku laboratoře s tzv. cílovou hodnotou (target value). Ta bývá určena buď pomocí referenční metody, nejlepší soudobé rutinní metody v síti referenčních laboratoří, nebo se za ni považuje aritmetický průměr či medián všech účastníků kontrolního cyklu po vyloučení odlehlých hodnot. Kontrolní limity (Dmax) externího posuzování kvality jsou povolené procentuální odchylky měření účastníků od cílových hodnot měřené veličiny. Určují se na podkladě biologických rozptylů analytů s přihlédnutím k soudobým analytickým možnostem. Příklad výsledku EHK pro jednu metodu ukazuje následující obrázek.
+
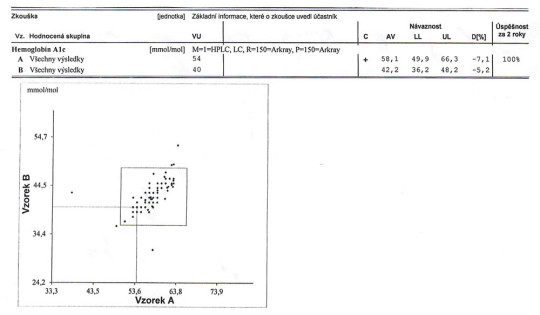
Ukázka výsledku externího hodnocení kvality pro glykovaný hemoglobin (hemoglobin A1c); VU = výsledek účastníka, C = hodnocení úspěšnosti zkoušky, AV = vztažná (cílová) hodnota, LL = dolní mez, UL = horní mez, D(%) = rozdíl VU a AV v procentech. V grafu dole body ukazují výsledky všech testovaných laboratoří; úspěšné laboratoře by měly mít body uvnitř čtverce, souřadnice ukazují bod testované laboratoře
3.7.3
Další požadavky na kvalitu práce laboratoře
Diskutovaná kontrola kvality laboratorního vyšetření je součástí širší problematiky označované pojmem správná laboratorní práce (SLP) – good laboratory practice (GLP). Sem také patří:
- kontrola preanalytických vlivů;
- organizace práce a manipulace se vzorky, vylučující záměnu vzorků;
- objednávání a zajišťování kvalitních reagencií i přístrojů;
- správná dokumentace výsledků;
- správná interpretace výsledků a další postanalytické faktory.
Systém SLP proto musí zahrnovat a obsáhnout prakticky vše, co souvisí s chodem laboratoře (personální otázky, organizační postupy, plánování, bezpečnost práce, provádění analýz, sledování funkce přístrojů, údržbu přístrojů, kontrolu kvality metod, zaznamenávání výsledků, interpretaci výsledků, komunikaci s klienty i dodavateli aj.).
Jednou z hlavních zásad systému SLP je, že veškerá činnost prováděná v laboratoři i veškeré údaje a výsledky produkované laboratoří musí být precizně a podrobně dokumentovány formou řízené dokumentace. Jejím cílem je, aby každá činnost byla dokonale popsána a definována právě v jednom aktuálním dokumentu (příručka jakosti, laboratorní příručka, standardní operační postup analytický, technický, organizační či statistický, karta pracovníka, karta přístroje, výsledky mezilaboratorních kontrol atd.).
Laboratorní postupy musí být validovány a verifikovány. Validace je proces, kterým se získávají objektivní důkazy, že metoda, postup či přístroj vykazují vlastnosti, jež jsou k danému použití požadovány. Přestože jsou výrobky před uvedením na trh validované výrobcem, musí být před uvedením do provozu znovu verifikovány (verifikace = zkrácená validace), aby bylo ověřeno, že validační údaje výrobce platí i v konkrétních podmínkách laboratoře.
Problematika certifikace a akreditace laboratoře bude zmíněna v kapitole 27.
Celkově lze shrnout, že SLP a systém řízení kvality nepředstavují jednorázovou činnost, ale nepřetržitý proces vedoucí ke stálému zlepšování kvality činnosti laboratoře, do kterého musí být trvale a odpovědně zapojeni všichni pracovníci laboratoře.
Souhrn
Kapitola rozebírá čtyři základní analytické vlastnosti: preciznost, pravdivost, analytickou senzitivitu a analytickou specifičnost. Je popsáno ovlivnění těchto vlastností jednotlivými druhy chyb a vysvětlen pojem nejistoty měření. Dále je popsána kontrola kvality laboratorního vyšetření (externí, interní) a zásady jejího správného provádění. Kapitola končí vysvětlením pojmů správná laboratorní práce, řízená dokumentace a validace a verifikace metody.
Student vysvětlí pojmy preciznost, pravdivost, analytická senzitivita a analytická specifičnost a uvede jejich vztah k jednotlivým druhům chyb. Zdůvodní význam nejistoty měření pro interpretaci výsledku. Popíše správné zásady kontroly kvality laboratorního vyšetření a způsob provádění v praxi včetně užití regulačního grafu v interní kontrole kvality a vysvětlí jednotlivé parametry a grafy v dokumentu z externího hodnocení kvality v ČR. Vysvětlí rozdíl mezi validací a verifikací metody.
Preciznost metody zhoršují chyby
Interference látek přítomných ve vzorku způsobuje chybu
Opakování analýzy téhož vzorku
Mimo rozmezí x̄ ± 2s může ležet následující procento výsledků kontrolních vzorků