Zkumavkové testy s tekutými činidly se v běžném rutinním vyšetřování moče používají jen velmi vzácně a přednost se dává diagnostickým proužkům různých výrobců.
Postup práce s diagnostickými proužky:
Vždy vyšetřujeme pouze čerstvou (ne starší 4 hodin) moč, dobře promíchanou, bez přítomnosti konzervačních prostředků, odebranou do čisté nádoby bez stop desinfekce a detergentů.
Z tuby vyjmeme potřebný počet proužků, aniž bychom se dotýkali prsty reagenčních zón proužků. Tubu s ostatními proužky uzavřeme originální zátkou se sušidlem. Proužek krátce (cca na 1 – 2 sekundy) ponoříme do moči, otřeme kapku o okraj nádoby a přebytečnou moč ještě odstraníme otřením hrany proužku o buničinu, aby se zabránilo smíchání činidel z jednotlivých reagenčních zón. Proužek položíme na vodorovnou podložku a srovnáme zabarvení příslušné zóny (zóny pH srovnáváme IHNED, zóny jiných patologických součástí pak podle návodu, zpravidla po 1 minutě) s barevnou stupnicí na štítku tuby nebo vyhodnotíme zabarvení jednotlivých zón pomocí reflexního fotometru.
POZOR! Zbarvení zkresluje přítomnost par amoniaku v ovzduší laboratoře.
Diagnostické proužky se skladují v uzavřených původních obalech na suchém místě při (+2 až +30) °C. Proužky je nutné chránit před účinkem vzdušné vlhkosti, přímého slunečního světla, zvýšené teploty a chemických výparů v laboratoři.
Stanovení pH moči
Udržování stálého pH, tj. udržování acidobazické rovnováhy je základní podmínkou životních procesů. Acidifikační a alkalizační funkce ledvin se odráží v pH moče. Stanovení pH provádíme co nejdříve, aby nedošlo k rozmnožení mikroorganizmů, které je spojeno s tvorbou amoniaku (vzniká rozkladem močoviny) a tím i ke zvýšení pH.
Pokud není moč infikovaná, je hodnota pH moči uchovávané v chladničce 4 i více hodin stabilní.
Referenční hodnoty: 5 – 6,5
pH je ovlivněno potravou. Při bílkovinné stravě je pH nízké (kyselá moč), při vegetariánské stravě je pH neutrální až mírně alkalické.
nízké pH (acidurie): pH < 5
Příčiny:
fyziologicky: při masité stravě
patologicky:
- respirační (neschopnost vyloučit CO2) a metabolická acidóza
- dna
pH < než 4,5 neznáme
vysoké pH (alkalurie): pH > 6,5 (někdy i vyšší než 9)
Příčiny:
fyziologicky: laktovegetabilní strava, přechodně po vydatném jídle
patologicky:
- horečka
- infekce močových cest (rozklad močoviny na amoniak)
- respirační alkalóza (vydýchání hodně CO2)
- metabolická alkalóza
Největší význam má stanovení pH moči pro diagnostiku a léčbu močové infekce a urolitiázy.
STANOVENÍ pH diagnostickými proužky PHAN firmy Erba Lachema
Zóny obsahují chromogeny (směsné acidobazické indikátory, tj. bromthymolová modř + methylčerveň), které se zabarvují nebo změní barevný odstín v závislosti na změnách koncentrace H+ od oranžové, přes žlutou a zelenou až do modré, rozmezí pH 5 – 9. Přesnost měření je pouze ± 0,5 pH.
Falešně pozitivní výsledky: přítomnost formaldehydu způsobuje falešně nižší pH, stará moč falešně vyšší pH
Poznámka
- Některé z acidobazických indikátorů v přítomnosti bílkoviny vykazují zbarvení odpovídající vyššímu pH než je hodnota skutečná. Vzniká tzv. proteinová chyba indikátoru. Tohoto nežádoucího jevu se využívá k důkazu bílkoviny.
- V případě potřeby přesnějšího stanovení pH moči je možné provést měření pH pomocí pH-metru (potenciometrické měření).
Proteinurie je stav, při kterém jsou běžné zkoušky na přítomnost bílkoviny v moči pozitivní.
Referenční hodnoty:
< 0,2 g/24 h, což za normálních okolností běžnými zkouškami neprokážeme
< 0,1 g/l (max. 0,2 g/l)
Hlavní složkou fyziologické proteinurie je albumin.
Příčiny proteinurie:
- Přechodné proteinurie:
- Patologické proteinurie:
Nejčastějšími příčinami jsou chronické záněty ledvin, nefrózy, diabetes mellitus, těžké srdeční a cévní choroby, požití toxických látek a léčiv (př. sulfonamidy, opiáty, barbituráty, sloučeniny rtuti a kadmia aj.), prerenální proteinurie např. u hemolýzy, poškození velkého množství svalů či u pacientů s mnohočetným myelomem (tzv. Bence-Jonesova bílkovina).
Metody stanovení proteinurie:
- diagnostickými proužky
Princip:
Využívají proteinovou chybu speciálního indikátoru, který se při pH < 3,5 barví jasně žlutě. Při pH vyšším dochází ke změně zbarvení přes zelenou až do modré. pH < 3,5 zajišťuje pufr obsažený v indikační zóně. V přítomnosti bílkoviny uvolňuje indikátor (př. etylester tetrabromfenolftaleinu) H+,
+
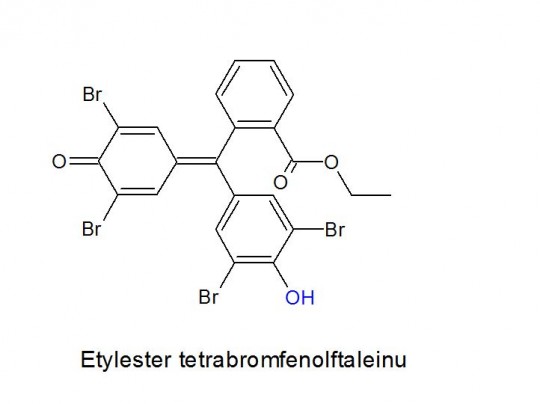
Obr. 14. Etylester tetrabromfenolftaleinu
bílkoviny se naváží na indikátor svými aminoskupinami, tím se posune přechodová oblast indikátoru ke kyselejšímu pH. Zbarvení indikátoru s navázanou bílkovinou při konstantním pH < 3,5 přechází ze žluté do zelena až modra jako při zvýšení pH.
Tzn.: pH < 3,5 zajišťuje pufr. Je-li moč bez bílkoviny ⇒ jasně žlutá zóna
s bílkovinou ⇒ zelená až modrá zóna (jakoby došlo ke zvýšení pH a nikoliv k přídavku bílkovin)
Hodnocení se provádí porovnáním s barevnou škálou na tubě nebo pomocí reflexního fotometru.
Citlivost proužků: 0,3 g/l
Proužky jsou citlivé hlavně na albumin, podstatně méně na globuliny, mukoproteiny, hemoglobin a Bence-Jonesovu bílkovinu.
Stanovení sice není ovlivňováno hodnotou pH, ale při pozitivním výsledku a pH > 8,0 okyselíme zředěnou kyselinou octovou na pH = 5 – 6 a stanovení opakujeme, protože někdy moče s vysokou tlumivou kapacitou nebo s extrémně alkalickým pH dávají falešně pozitivní výsledky i v nepřítomnosti bílkovin.
Chybné výsledky:
- při dlouhodobém ponoření proužku (dojde k vymytí pufru, proužek pak indikuje změnu pH a nikoliv proteinurii)
- zbytky dezinfekčních činidel nebo konzervačních prostředků ve sběrných nádobách, kontaminace bílkovinou pocházející z vaginálního sekretu nebo ejakulátu, vaječný bílek (úmyslně přidán do moče) způsobují falešnou pozitivitu
- moče pacientů, kterým byly podávány chininové preparáty nebo léčiva na bázi derivátů chinolinu, alkaloidy apod., mohou dávat falešně pozitivní výsledky
- falešnou negativitu způsobuje přítomnost jiného proteinu než albuminu (globuliny, lehké řetězce imunoglobulinů) a neionogenních nebo anionaktivních detergentů
V případě pozitivního nálezu při pH > 8 provádíme pro ověření výsledku další zkoušku:
- Stanovení bílkovin kyselinou sulfosalicylovou
Princip stanovení:
Bílkoviny se v moči vysráží kyselinou sulfosalicylovou, což se projeví zákalem ev. až sraženinou. Pokud není moč čirá, vzniklý zákal porovnáme se zákalem ve druhé zkumavce, ve které jsme nechali 1/2 z původního množství moči a kterou pouze okyselíme kapkou kyseliny octové.
Reagencie: 20% roztok kyseliny sulfosalicylové
Provedení: Ke 2 – 3 ml čiré nebo přefiltrované moči přidáme 3 – 5 kapek 30% kyseliny octové (upravení pH ≈ 4,6). Pak přidáme po kapkách asi 10 kapek 20% kyseliny sulfosalicylové. Vzniklý zákal hodnotíme proti tmavému pozadí a v bočním světle (jinak mohou vzniknout chyby).
koncentrace bílkovin [g/l] | hodnocení v arbitrárních jednotkách | hodnocení křížky | |
bez zákalu | < 0,1 | 0 | negativní |
zákalem lze číst text | 0,1 – 0,25 | 1 | + |
nelze číst text (ale bez vloček) | 0,25 – 2,0 | 2 | ++ |
mléčný zákal až vločky | 2 – 4 | 3 | +++ |
tvarohovitá sraženina | > 4 | 4 | ++++ |
Vadí: konzervace thymolem
Stanovení ruší: sulfonamidy, penicilin, kontrastní jodové preparáty (vyloučené do moči)
Glykoproteiny, k jejichž zvýšenému vylučování dochází u zánětlivých procesů, se však touto metodou nesráží a tedy nezachytí. Zachytí se však i fyziologická proteinurie (od 20 mg/den), která se projeví opalescencí.
Glukóza je nejčastějším cukrem v moči, ostatní cukry jsou méně časté. Do moče se dostává z krevního oběhu glomerulární filtrací. Většina glukózy je však v ledvinových tubulech vstřebávána zpět do krve. Kapacita tubulárních buněk pro resorpci glukózy je 8 – 11 mmol/l v plazmě, tzv. ledvinový práh pro glukózu. Je-li ledvinový práh překročen, glukóza se dostává do moče. Při posuzování výsledků je nutno mít na paměti, že renální práh pro glukózu má značné individuální kolísání. Jeho orientační vyšetření lze provést perorálním podáním glukózy, stanovením glykémie a zároveň průkazem glukózy v moči. U diabetiků může být renální práh zvýšen až na hodnoty 14 – 16 mmol/l.
Glykosurie = cukry v moči (správnější je rozlišovat: glukosurii, fruktosurii, laktosurii atd.)
- Prerenální: je překročen ledvinový práh pro glukózu ⇒ glukóza přechází do moči
Příčina:
- alimentární glykosurie (požitím velkého množství glukózy, kdy glykémie překročí hodnotu ≈ 10 mmol/l po dobu ≥ 15 min)
- při nesprávné rychlosti podávání glukózy při infuzi
- diabetes mellitus
- Renální: je snížen ledvinový práh pro glukózu (pod 9 mmol/l) ⇒ ↑glykosurie, ale normální hodnoty glykémie
Příčina:
- těhotenství
- renální onemocnění (porucha ledvinných tubulů)
- toxické poškození ledvin (např. otrava rtutí)
Další příčiny glykosurie:
- závažné poruchy jater (cirhóza, infekční žloutenka)
- nitrolební nádory
- nádory dřeně nadledvin
- podání adrenalinu, ACTH aj. kortikoidů
- akutní pankreatitida aj.
Referenční hodnoty glykosurie: 0,1 – 0,8 mmol/l v ranní moči
(někdy se uvádí do 0,56 mmol/l), což je pod prahem citlivosti většiny metod. Je-li koncentrace < 0,1 mmol/l, jde pravděpodobně o zvýšenou bakteriurii (přítomnost bakterií, které metabolizují glukózu).
Při stanovení glukózy ve sbírané moči se moč sbírá po dobu 6, 8, 12 nebo 24 hodin do sběrné nádoby bez přídavku konzervačních látek. Při sběru moče je nutné zabránit bakteriální kontaminaci, moč se uchovává v chladničce. Před odlitím vzorku moči ze sběrné nádoby se moč důkladně promíchá a změří se její objem s přesností na 10 ml (u velmi malých dětí s přesností na 1 ml).
METODY STANOVENÍ GLUKÓZY
Stanovení diagnostickými proužky
Princip metody:
Glukóza se oxiduje vzdušným kyslíkem na kyselinu glukonovou za katalytického působení glukózooxidázy. Při reakci se uvolňuje peroxid vodíku, který oxiduje nebarevnou formu chromogenu (tetrametylbenzidin) na oxidovanou zeleně zbarvenou formu (benzidinová modř). Reakci katalyzuje peroxidáza.
+
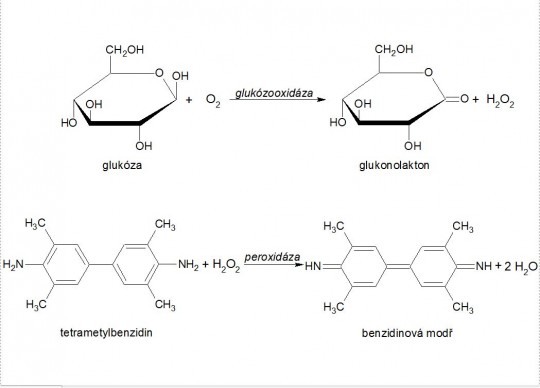
Obr. 15. Princip stanovení glukózy
Hodnocení:
Srovnáme zbarvení se stupnicí na obalu po 1 min.
Citlivost: ≈ 2 mmol/l
Falešně pozitivní výsledky:
- při znečištění nádob oxidačními prostředky, které se používají k dekontaminaci nádob pro sběr moče (př. chloramin, persteril)
- uchovávání proužků v otevřených tubách
Falešně negativní výsledky:
- nadměrná koncentrace vitaminu C v moči, která je způsobena i užíváním vitaminových tablet a směsí, dále např. infuzemi obsahujícími vitamin C
- kyselina homogentisová (alkaptonurie)
- dlouhá doba transportu
- brzká doba odečtu (< 1 min)
- močová infekce
- léčba antibiotiky, salicyláty apod.
Diagnostické proužky jsou pro glukózu specifické. Přítomnost jiných cukrů (galaktóza, fruktóza, pentózy) nevede ke zbarvení.
Při podezření na neglukózovou glykosurii (např. u novorozenců) se obvykle provádí orientační Benediktova zkouška, k upřesnění (galaktosurie, fruktosurie) se pak využívají složitější specifické metody.
Princip metody:
Glukóza redukuje za varu měďnatou sůl v alkalickém prostředí za přítomnosti uhličitanu sodného a citronanu sodného na oxid měďný (Cu2O), jehož disperze charakteristicky zbarví roztok. Po ochlazení se hodnotí modré a zelené zbarvení čirého obsahu zkumavky nebo zelená, oranžová až červená sraženina. Výsledek se uvádí v arbitrárních jednotkách (+, ++, atd.).
Před prováděním redukčních zkoušek je nutno zjistit, zda moč neobsahuje bílkovinu, která má také redukční vlastnosti. Jestliže je bílkovina v moči přítomna, je nutná deproteinace (např. varem) a bílkovinu následně odstranit např. filtrací nebo centrifugací. Další stanovení glukózy je prováděno ve filtrátu resp. v supernatantu.
Reagencie:
- Benediktovo činidlo:
- 17,3 g CuSO4 . 5 H2O rozpustit ve 100 ml vody
- 100 g bezvodého Na2CO3 a 173 g citronanu sodného p.a. rozpustit v 700 ml destilované vody
Roztok a) a b) přefiltrovat do 1 000 ml odměrné baňky, promíchat a doplnit po rysku.
Pro deproteinaci se připraví:
- octanový pufr o c = 2 mol/l a pH = 4,6
60 ml ledové kyseliny octové p.a. smícháme se 125,2 g CH3COONa . 3 H2O a doplníme destilovanou vodou do 1 000 ml.
Provedení:
- Obsahuje-li moč bílkovinu, provede se deproteinace: 5 ml moče + 1 ml octanového pufru povařit, sraženinu odfiltrovat a dále pracovat s filtrátem
- 2,5 ml Benediktova činidla + 4 kapky (0,1 ml) moče po deproteinaci
- Promíchat a 1 – 2 min vařit nad malým plamenem (OPATRNĚ, za stálého protřepávání – alkalické roztoky snadno vzkypí!) nebo 5 minut ve vroucí vodní lázni, vychladit a vyhodnotit
Hodnocení:
Nález | Hodnocení v arbitrárních jednotkách | Přibližná hmotnostní koncentrace glukózy [g/l] | Přibližná látková koncentrace glukózy [mmol/l] |
modrý, čirý roztok | negativní | < 0,8 | < 4,5 |
zelený roztok bez sraženiny | 1 nebo ± | 1 – 3 | 5 – 20 |
zelená sraženina | 2 nebo + | 5 – 10 | 25 – 30 |
olivově zelená sraženina | 2 nebo ++ | cca 10 – 15 | 50 – 60 |
oranžová sraženina | 3 nebo +++ | cca 15 | 70 – 90 |
červená sraženina | 4 nebo ++++ | 20 a více | 100 – 120 |
Benediktova zkouška není pro glukózu specifická, reagují i jiné redukující cukry a redukující látky. Nesprávně pozitivní výsledky jsou např. v přítomnosti zvýšené koncentrace kyseliny močové, vitaminu C, salicylátů a dalších redukujících látek.
Stanovení žlučových barviv v moči
Mezi žlučová barviva zařazujeme:
- bilirubin
- urobilinogen, sterkobilinogen – tzv. Ehrlich pozitivní látky
- urobilin, sterkobilin – tzv. Schlesinger pozitivní látky
- bilirubin
Za patologických stavů se v moči nachází bilirubin konjugovaný (přímý).
Zvýšené hodnoty:
- obstrukční ikterus (kámen, nádor žlučových cest)
- parenchymatózní ikterus (virová hepatitida, infekční mononukleóza, cirhóza jater, toxické poškození jater např. CCl4).
Nekonjugovaný bilirubin (nepřímý) stoupá v krvi u hemolytických žloutenek a parenchymatózního ikteru, ale do moči neproniká. V moči se vyskytuje vzácně, např. při kombinaci hemolytického ikteru se současnou poruchou ledvin, u které je zvýšená permeabilita glomerulární membrány.
Stanovení bilirubinu diagnostickými proužky
Princip metody:
Bílá zóna obsahuje činidlo (stabilizovaná diazoniová sůl) poskytující s bilirubinem v kyselém prostředí růžové až karmínově červené zbarvení.
+
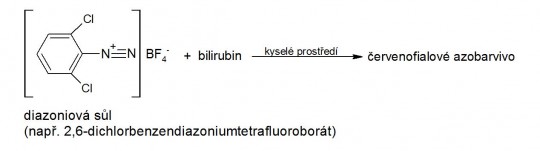
Obr. 16. Princip stanovení bilirubinu
Reakce není ovlivněna hodnotou pH moče. Interferují vysoké koncentrace urobilinogenu (nad 100 μmol/l) a látky, které jsou červeně zbarveny nebo se barví červeně vlivem kyselého prostředí reagenční zóny.
Vyšetřované vzorky nesmí být vystaveny přímému slunečnímu záření, které vyvolává oxidaci bilirubinu a způsobuje falešně nižší až falešně negativní výsledky.
- urobilinogen a sterkobilinogen
Urobilinogen a sterkobilinogen se označují společným názvem „urobilinogen“. Označují se také jako Ehrlich pozitivní látky, neboť poskytují s Ehrlichovým aldehydickým činidlem (p-dimethylaminobenzaldehyd a HCl) červený komplex.
Urobilinogen vzniká redukcí bilirubinu působením bakteriální flóry střeva. Moč s vysokou koncentrací urobilinogenu má hnědočervené zbarvení, které se na vzduchu mění na oranžové (urobilin). Urobilinogen se netvoří při chybění střevní flóry (fyziologicky u novorozenců, při razantní ATB léčbě), naopak největší vylučování nastává asi za 4 h po větším jídle.
↑ koncentrace:
- fyziologicky po nadměrném požití velkého množství masa, zeleniny
- při funkčním zatížení nebo nedostatečnosti hepatocytů (virová hepatitida, cirhóza, toxické poškození jater, hemolytický ikterus, hemolytická anémie, nádory) – urobilinogen se nepřesně označuje jako „pigment nemocných jater“
↓ koncentrace:
při uzávěru žlučových cest a při úplné zástavě odtoku žluči může urobilinogen úplně chybět (u obstrukčního ikteru je nález negativní!!!)
Stanovení urobilinogenu diagnostickými proužky:
Princip metody:
Reakční zóna proužku obsahuje aromatickou diazoniovou sůl v kyselém pufru, která reaguje s urobilinogenem za vzniku růžového až karmínově červeného azobarviva.
V přítomnosti bilirubinu se reagenční zóna barví žlutě. Toto zabarvení, které přechází po 1 minutě do modrozeleného zbarvení, v zásadě nebrání stanovení urobilinogenu za předpokladu dodržení odečítacího času. Z ostatních případných součástí moče interferují pouze látky, které jsou červeně zbarveny nebo se barví červeně vlivem kyselého prostředí reagenční zóny (př. některé léky).
Falešnou pozitivitu mohou způsobit dusíkaté metabolity bakterií u některých močových infekcí, falešnou negativitu pak vysoké koncentrace vitaminu C, zvýšení nitritů, pozdní dodání vzorku do laboratoře nebo vliv světla.
Poznámka
- reakce není ovlivněna hodnotou pH moče
- stanovení se provádí jen v čerstvé moči!
- reakce je pro urobilinogen a sterkobilinogen specifická
- moč je nutno chránit před slunečním světlem, které vyvolává fotooxidaci urobilinogenu a způsobuje falešně nižší až falešně negativní výsledky
- urobilin a sterkobilin
Urobilin i sterkobilin se močí nevylučují. Vznikají v ní oxidací urobilinogenu a sterkobilinogenu. Jsou přítomny v močích déle stojících na vzduchu a světle.
Označují se jako Schlesinger pozitivní látky.
Vylučování ketolátek močí se označuje jako „ketonurie“.
Ketolátky (podle nové nomenklatury oxolátky) jsou intermediární metabolity zahrnující kyselinu 3-hydroxymáselnou (tvoří 60 – 70 % všech ketolátek), kyselinu acetoctovou (30 – 35 % ketolátek) a aceton (zastoupen jen několika procenty).
+
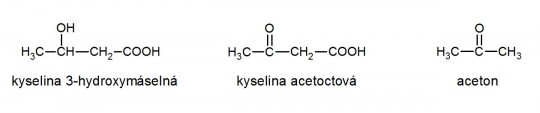
Obr. 17. Ketolátky: kyselina 3-hydroxymáselná, kyselina acetoctová a aceton
Vznikají v játrech jako meziprodukt při metabolizmu lipidů (oxidací mastných kyselin).
Průkaz ketolátek v moči má význam hlavně pro včasné rozpoznání metabolické dekompenzace diabetiků. Za normálních okolností, pokud pacient nehladoví, je koncentrace ketolátek pod prahem citlivosti užívaných metod.
Příčiny ↑ koncentrace ketolátek v moči:
- hladovění – př. u redukčních diet, které lze průkazem ketolátek v moči kontrolovat (zásoba jaterního glykogenu je vyčerpána, sacharidy se nepřijímají a nastává štěpení tuků)
- nedostatečný příjem glycidů při nadměrném výdeji energie (námaha + redukční dieta)
- horečnaté stavy
- dlouhodobé zvracení + průjmy (ketonické zvracení dětí)
- diabetická ketoacidóza (ketonurie + hyperglykémie u diabetu mellitu 1. typu). Vázne přeměna glukózy, potřeba energie se kryje odbouráváním mastných kyselin. Vzniká tak větší množství ketolátek, které organizmus nestačí zpracovat na vodu a CO2. Jejich hladina v krvi vzrůstá a vylučují se do moči. Diabetická ketoacidóza je znakem, že nemoc je nesprávně léčena.
Stanovení ketolátek v moči diagnostickými proužky
Princip metody:
Základem je Legalova reakce. Indikační zóna obsahuje nitroprusid sodný v silně alkalickém prostředí. Na přítomnost ketolátek (zejména kyselinu acetoctovou, méně na aceton) reaguje indikátor změnou zbarvení z krémového přes růžovou do temně fialové.
+
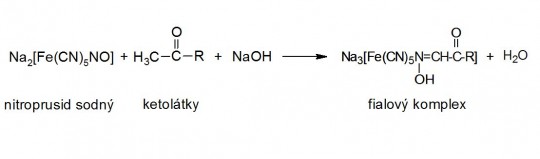
Obr. 18. Legalova reakce
Test je citlivý hlavně na kyselinu acetoctovou, méně na aceton. S kyselinou 3-hydroxymáselnou (tedy nejhojněji zastoupenou ketolátkou) test nereaguje, a proto i při negativním výsledku není ketoacidóza zcela vyloučena.
Poznámka
- Barevná stupnice je kalibrována na koncentraci kyseliny acetoctové.
- Falešnou pozitivitu může způsobit přítomnost kyseliny fenylpyrohroznové (u fenylketonurie) nebo léčiva na bázi fenolftaleinu nebo sulfonftaleinu.
- K falešné negativitě může vést tkáňová hypoxie u pacientů v šokovém stavu (kyselina 3-hydroxymáselná nereaguje), dlouhá doba transportu vzorku, odběr z močového vaku (odpaření ketolátek).
Za normálních okolností se krevní barvivo v moči nevyskytuje.
Nález krve v moči nazýváme hematurie.
Hematurie:
- erytrocyturie
Erytrocyturii nacházíme např. při zánětu ledvin, tuberkulóze ledvin, močových kamenech, hemofilii, skorbutu, po úrazech a operacích na močových cestách, při karcinomu prostaty, infarktu ledviny, při některých infekčních a oběhových chorobách.
- Při výrazných poruchách ultrastruktury glomerulů (glomerulonefritida, maligní hypertenze, nefrotický syndrom, nefrotoxické látky aj.) ⇒ ↑proteinurie.
- Je-li erytrocyturie následkem nepříliš rozsáhlého krvácení v ledvinách nebo v močových cestách (poranění, urolitiáza, záněty nebo nádory močových cest aj.), může proteinurie zcela chybět.
- hemoglobinurie – hemoglobin v moči.
K hemoglobinurii dochází při všech stavech provázených intravaskulárním rozpadem erytrocytů – např. při akutní hemolytické anémii, při popáleninách, po velké fyzické námaze nebo vlivem chladu či horka (obvykle mizí do druhého dne), při otravách chlorečnany a některými houbami („hemolytické jedy“), při inkompatibilitě při transfuzích.
Chemicky nelze erytrocyturii a hemoglobinurii rozeznat (některé proužky to však dokáží, viz dále), erytrocyturii je však vždy nutné potvrdit vyšetřením sedimentu.
Hematurie:
- mikroskopická (skrytá, okultní) – nezjistitelná pouhým okem
- makroskopická – růžová až červená moč, přítomen červenavý až hnědavý zákal a červený sediment (erytrocyty)
Podle příčin se dělila hematurie na:
- prerenální (vždy hemoglobinurie) ↔ zvýšená hemolýza, otravy, sepse
- renální ↔ úrazy, nádory
- postrenální ↔ kameny, záněty
V současné době se častěji používá rozdělení hematurií na:
- glomerulární
- non-glomerulární
Stanovení krevního barviva diagnostickým proužkem
Diagnostický proužek je založen na průkazu hemu. Pozitivní reakci poskytuje volný hemoglobin, hemoglobin v erytrocytech a myoglobin (vylučuje se při rozpadu kosterního svalstva).
Princip metody:
Světle žlutá zóna obsahuje stabilizovaný organický hydroperoxid (způsobuje, že reakce nemůže být katalyzována peroxidázami leukocytů) a chromogen (tetrametylbenzidin), který se za přítomnosti hemoglobinu oxiduje na modře zbarvené produkty (tzv. pseudoperoxidázový účinek hemoglobinu).
chromogen-H2 + H2O2
oxidovaná forma chromogenu + 2 H2O
chromogen: tetrametylbenzidin apod.
+
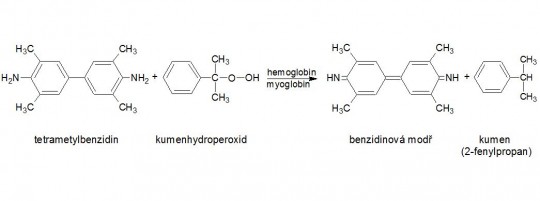
Obr. 19. Princip stanovení krevního barviva diagnostickým proužkem
Proč pseudoperoxidázová reakce?
Hemoglobin katalyzuje oxidace vhodných substrátů peroxidem vodíku, podobně jako enzym peroxidáza. Nejedná se však o enzymovou aktivitu. Hemoglobin ji neztrácí ani po tepelné denaturaci. Důkaz pseudoperoxidázové aktivity se má provádět v převařených vzorcích, aby se vyloučila případná enzymová katalýza peroxidázami z leukocytů.
Pro analýzu krve štítek obsahuje 2 stupnice:
- pro detekci intaktních erytrocytů (tečkovaná stupnice)
- pro detekci volného hemoglobinu (homogenně zbarvená stupnice).
Test je vysoce citlivý na hemoglobin a zachytí jeho přítomnost již od koncentrací odpovídajících cca 5 ery/1 μl.
Citlivost testu je ovlivňována hustotou moče, případně přítomností inhibitorů, které jsou součástí léků.
Chyby:
- falešně negativní výsledky: za přítomnosti redukujících látek (př. vitamin C) nebo urátů v příliš koncentrovaných močích
- falešně pozitivní výsledky:
- v přítomnosti železitých solí, jodidů nebo stop silně oxidačních prostředků
- peroxidázy některých druhů bakterií, kvasinek a plísní
Stanovení dusitanů v moči
Přítomnost dusitanů v moči svědčí pro uroinfekci.
Stanovení dusitanů diagnostickým proužkem
Test využívá konverzi dusičnanů na dusitany (nitrity) působením zejména Gramnegativních bakterií obsažených v moči. Barevná reakce je založena na principu modifikované Griessovy reakce (diazotace sulfanilamidu dusitany ve vzorku za vzniku diazoniové soli, která následně reaguje azokopulační reakcí s kopulačním činidlem za vývinu růžového až fialového zbarvení).
+
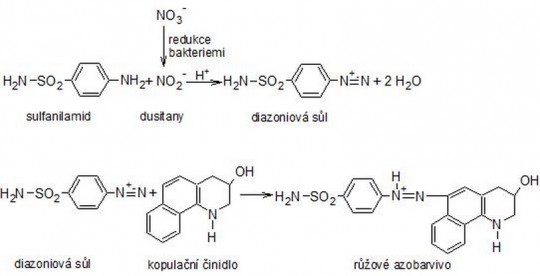
Obr. 20. Princip stanovení dusitanů diagnostickými proužky
Jakékoliv růžové zbarvení představuje jednoznačný důkaz kvantitativně významné bakteriurie, tj. přítomnost 105 nebo více organizmů v 1 ml moči, ale zbarvení zóny není kvantitativně úměrné množství přítomných bakterií v moči. Negativní výsledek však bakteriurii nevylučuje. Množství dusitanů v moči je závislé nejen na množství zárodků, ale i na jejich druhu, době působení a také na obsahu původně přítomných dusičnanů. Z těchto důvodů je test obecně považovaný za průkazný v přibližně 70 % všech bakteriurií (nenahrazuje mikrobiologické vyšetření!). Test je vhodné provádět vždy v první ranní moči, aby byla zajištěna dostatečná doba pro konverzi dusičnanů na dusitany bakteriemi přítomnými v moči.
Poznámka
- U novorozenců a kojenců do 5 měsíců nelze hodnotit. Výsledek je vždy negativní, protože nepřijímají dusičnany potravou. Stejně tak nelze test hodnotit při hladovění nebo parenterální výživě.
- Falešnou negativitu způsobuje vitamin C (ale obsah kyseliny askorbové 1000 mg/l nezpůsobí falešně negativní výsledky u močí s koncentrací dusitanů nad 2,5 mg/l), užívání antibiotik méně než 3 dny před odběrem.
- K falešné pozitivitě může vést dlouhá doba transportu (in vitro konverze dusičnanů na dusitany v důsledku arteficiální bakteriální kontaminace).
Stanovení leukocytů v moči
Přítomnost leukocytů v moči je důležitým příznakem zánětlivého onemocnění močových cest a ledvin (cystitida, pyelonefritida, glomerulonefritidy), ale i nádorů močových cest. Pro uroinfekci je typický nález alkalického pH, leukocytů, nitritů, bílkoviny, případně erytrocytů. Při masivní leukocyturii hovoříme o hnisu v moči, tzv. pyurii.
Stanovení leukocytů diagnostickým proužkem
Test je založen na enzymatické reakci, při které je působením enzymu esterázy (leukocytární elastáza) štěpen substrát na volný indoxyl. Ten dále reaguje s diazoniovou solí za vzniku růžového až fialového zbarvení. Intenzita tohoto zbarvení je úměrná množství leukocytů ve vzorku vyšetřované moče a hodnotí se po 120 s.
+
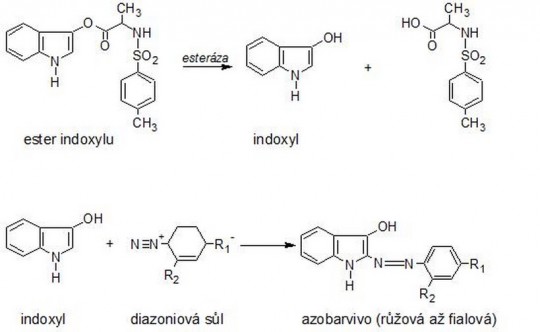
Obr. 21. Princip stanovení leukocytů diagnostickými proužky
Poznámka
- K rozpadu elementů dochází po 1 h od vymočení (zvlášť u hypotonické, alkalické, infikované moče), doporučuje se spíše 2. ranní moč.
- Jestliže má vzorek moče výraznější zbarvení (např. zvýšené množství bilirubinu), může být barevná odezva reakce tímto zbarvením zastřena.
- Intenzitu barevné reakce zvyšuje alkalické pH a vyšší hustota moče.
- Formaldehyd vede k falešné pozitivitě vyšetření.
Stanovení kyseliny askorbové v moči
Kyselina askorbová (vitamin C) se v moči objevuje při vysokém příjmu potravou a jako silné redukční činidlo může ovlivnit stanovení některých analytů v moči. Doporučuje se provést vyšetření moče na kyselinu askorbovou zejména v těch případech, ve kterých kyselina askorbová může ovlivnit testy na jiné složky moče jako glukózu, krev a dusitany.
Stanovení kyseliny askorbové diagnostickým proužkem
Test je založen na reakci kyseliny fosfomolybdenové, která se redukuje kyselinou askorbovou na molybdenovou modř. Test není specifický pro kyselinu askorbovou, protože i jiné silně redukující látky přítomné v moči jako např. kyselina homogentisová a metabolity kyseliny acetylsalicylové poskytují zelené až šedomodré zbarvení.
2.2.2
Kvantitativní vyšetření moči
V případě stanovení odpadu bílkovin, tj. celkového množství bílkovin ve sbírané moči (např. za 24 h) je nutná konzervace moči (př. azidem sodným).
V laboratoři se rutinně stanovuje koncentrace celkových bílkovin (udává se v g/l) a z ní se pak vypočítává celkový odpad bílkovin močí (udává se v g/d).
Referenční hodnoty: < 0,15 g/d (v ranní moči)
Výpočet DENNÍHO ODPADU BÍLKOVIN:
denní odpad bílkovin [g/den] = koncentrace [g/l] x objem moči [l/den]
Klinickobiochemický význam:
Nejčastější příčinou proteinurie je onemocnění ledvin, ale může k ní dojít i u jiných než ledvinových onemocnění.
Příčiny proteinurie (opakování):
- chronické záněty ledvin, horečnatá onemocnění, těžké choroby cév a srdce, nervové poškození
- požití toxických látek a léčiv (barbituráty, sulfonamidy, opiáty, Hg, Cd aj.)
- prerenální proteinurie např. u hemolýzy, poškození velkého množství svalů či u pacientů s mnohočetným myelomem (tzv. Bence-Jonesova bílkovina)
- febrilní proteinurie
- ortostatická proteinurie
- těhotenství, těžká tělesná zátěž (sport, pochody), po dlouhodobé expozici chladu vlivem sníženého prokrvení ledvin (př. studená koupel) a někdy před menses
Stanovení bílkoviny v moči pyrogallovou červení (Protein (Urine), souprava firmy BioSystems) [3]
Princip metody:
Proteiny tvoří v kyselém prostředí s pyrogallovou červení v přítomnost molybdenanu sodného červený komplex, který se měří fotometricky.
Složení činidel:
- Činidlo A (připraveno k použití) (4 x 50 ml) (pH = 2,3),
Pyrogallová červeň 60 μmol/l, molybdenan sodný 40 μmol/l, kyselina jantarová (sukcinát) 50 mmol/l
- Činidlo S (Standard) (1 x 5 ml),
hovězí albumin, koncentrace uvedena na štítku
Příprava pracovních roztoků:
Činidla jsou kapalná a určená k přímému použití.
Stabilita: I po otevření jsou stabilní do data exspirace uvedeného na obalu, pokud jsou skladována při teplotě 15 – 30 °C (činidlo A) a 2 – 8 °C (činidlo S) a chráněna před světlem a kontaminací.
Postup analýzy:
Vlnová délka 600 nm (590 – 610) nm, kyveta 1 cm, teplota 37 °C
Vzorky: sbíraná moč (moč se sbírá po dobu 24 h), skladuje se při 2 – 8 °C, změří se její objem a vzorek moči se uchovává při 2 – 8 °C. Vzorek je stabilní 8 dní.
Odměřit [ml] | Vzorek | Standard | Reagenční blank |
Sérum | 0,02 | --- | --- |
Činidlo S (Standard) | --- | 0,02 | --- |
Destilovaná voda | --- | --- | 0,02 |
Činidlo A | 1,00 | 1,00 | 1,00 |
Promíchá se a inkubuje 10 min při 37 °C. Změří se absorbance vzorku (Avz) a standardu (Ast) proti reagenčnímu blanku. Zbarvení je stabilní 30 minut.
Výpočet:
Bílkovina [mg/24 h] =
objem moči za 24 h
kde cst = koncentrace standardu v mg/l.
Poznámka
- Detekční limit: 70 mg/l.
- Limit linearity: 4000 mg/l. Při naměření vyšších koncentrací je nutno vzorek ředit v poměru 1 + 1, zopakovat měření a výsledek násobit 2x.
- Bilirubin do koncentrace 341 μmol/l a hemoglobin do koncentrace 0,63 g/l neinterferuje. Interferovat mohou některé léky.
Bezpečnostní charakteristiky:
Činidlo A:
Standardní věta o nebezpečnosti:
H 302 Zdraví škodlivý při požití
H312 Zdraví škodlivý při styku s kůží
H332 Zdraví škodlivý při vdechování
H341 Podezření na genetické poškození
Pokyny pro bezpečné zacházení:
P261 Zamezte vdechování prachu, dýmu, plynu, mlhy, par, aerosolů
P280 Používejte ochranné rukavice/ochranný oděv/ochranné brýle/obličejový štít.
P281 Používejte požadované osobní ochranné prostředky
P302 + P352 PŘI STYKU S KŮŽÍ: Omyjte velkým množstvím vody a mýdla.
P304 + P340 Při vdechnutí přeneste osobu na čerstvý vzduch a ponechte ji v poloze usnadňující dýchání
P308 + P313 Při expozici nebo podezření na ni vyhledejte lékařskou pomoc/ošetření
První pomoc:
Při náhodném požití vypláchnout ústa vodou, vypít asi 0,5 l vlažné vody. Při potřísnění pokožky nebo vniknutí do oka se pokožka nebo oko vypláchnou proudem čisté vody. Postiženému zajistíme kvalifikovanou lékařskou pomoc.
2.2.3
Morfologické vyšetření moče (močový sediment)
Sběr moči musí být proveden do naprosto čistých nádob. Doporučuje se odběr středního proudu druhé ranní moči. Ve vzorku první ranní moči mohou být buněčné elementy poškozené nebo už rozpadlé. Zpracování moči má být provedeno co nejdříve po odběru (max. do 1 h), protože některé součásti močového sedimentu se při pokojové teplotě rychle rozpadají.
Jedním z předpokladů získání spolehlivých výsledků je důsledné dodržování standardních podmínek při přípravě mikroskopických preparátů.
Příprava nativního preparátu:
Odebraný vzorek moči dobře promícháme. Odměříme vždy konstantní objem moči (př. 10 ml), který centrifugujeme 5 – 10 min při 1000 – 2000 ot./min (další zvyšování otáček by mohlo způsobit poškození buněčných elementů a válců). Opatrně odsajeme 9 ml supernatantu. Zbývající objem (1 ml) ve zkumavce promícháme, na čisté podložní sklíčko přeneseme kapku sedimentu a přikryjeme krycím sklíčkem tak, aby nevznikly vzduchové bublinky. Preparát nejdříve prohlížíme v mikroskopu při malém zvětšení (50 – 100 krát) pro získání celkového orientačního přehledu. Potom prohlížíme preparát při větším zvětšení (400 krát), které nám umožní identifikovat a počítat jednotlivé složky močového sedimentu.
Pro lepší rozlišení některých součástí močového sedimentu se močový sediment může obarvit. Nejčastěji se používá tvz. supravitální barvení dle Sternheimera (alciánová modř a červeň Pyronin B v poměru 1:1). K 1 kapce (50 μl) barviva se přidá 0,5 ml sedimentu, jemně se promíchá a po pěti minutách se provede mikroskopické vyhodnocení.
Minimálně deset polí stačí prohlédnout tehdy, je-li:
- četnost jednotlivých součástí velká;
- rozptyl jednotlivých součástí rovnoměrný.
V opačných případech je nutné prohlédnout celou plochu preparátu.
Výsledek se vyjadřuje jako počet elementů v 1 μl (mm3) moči. Pro zvýšení přesnosti při zjišťování počtu částic se používá Bürkerova nebo jiná počítací komůrka (např. destičky Fast-Read 102).
Erytrocyty
jsou kulovité, ostře ohraničené bezjaderné útvary s projasněným středem.
+
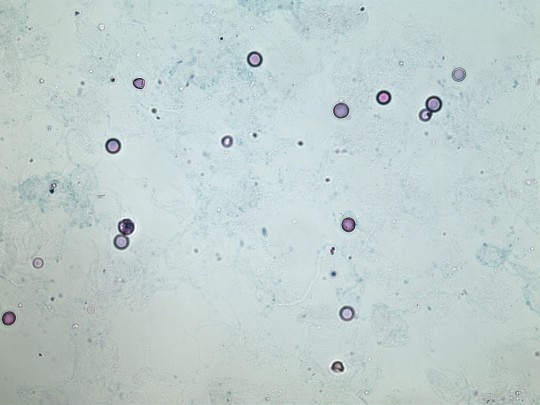
Zdroj: Autor Ing. Ivana Hupáková, Erytrocyty, licence Creative Commons BY-SA 4.0.
Obr. 22. Erytrocyty (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
V koncentrované (hypertonické) moči a v silně kyselé moči se svrašťují a podobají se ostnatým plodům kaštanu. V hypotonické moči se barvivo vyluhuje a erytrocyty se stávají téměř bezbarvými, někdy i obtížně viditelnými útvary – tzv. erytrocytovými stíny.
Do moči se mohou erytrocyty dostat průchodem glomerulární membránou. Dochází tím k deformaci jejich tvaru (dysmorfní erytrocyty). Zvýšený výskyt dysmorfních erytrocytů je typickým nálezem při postižení ledvinných glomerulů. V moči také můžeme nalézt erytrocyty, které mají původ v močových cestách nebo v ledvinách (prasklé cévy u nádorů, močové kameny, poranění ledvin apod.). U těchto erytrocytů k deformaci tvaru nedochází (izomorfní erytrocyty). Poškozené erytrocyty se nejlépe pozorují mikroskopem s fázovým kontrastem.
Příčinou zvýšeného množství erytrocytů v moči může být i podchlazení, přehřátí, extrémní fyzická námaha nebo příměs menstruační krve.
Leukocyty
Jsou tvarově závislé na pH. Ve slabě alkalické, neutrální nebo kyselé moči tvoří kulaté útvary větší než erytrocyty, se segmentovaným jádrem uprostřed. Jedno nebo více jader je vidět u barvených preparátů.
+
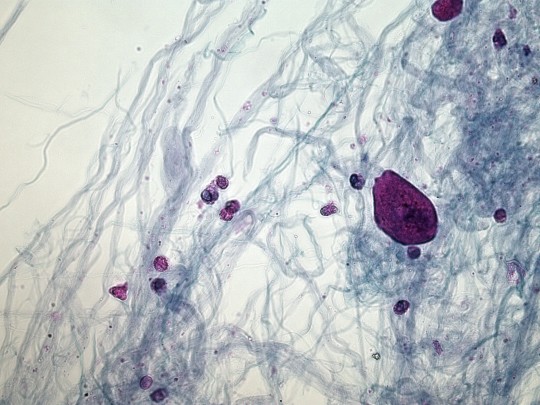
Zdroj: Autor Ing. Ivana Hupáková, Leukocyty, hlen, licence Creative Commons BY-SA 4.0.
Obr. 23. Leukocyty, hlen (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
V alkalické moči se leukocyty zvětšují, v silně alkalické moči se rozrušují.
Přítomnost leukocytů je typická pro bakteriální záněty močových cest nebo ledvin, ale vyskytuje se i u nádorů močových cest a močového měchýře. Důvodem nálezu více leukocytů v sedimentu než odpovídá semikvantitativnímu chemickému stanovení diagnostickými proužky je, že indoxyl-esterázovou reakcí se stanovují téměř výhradně neutrofilní granulocyty. Reagenční zóna na diagnostickém proužku lymfocyty nedetekuje. Současný nález leukocyturie, proteinurie a leukocytárních válců svědčí pro infekci ledviny (pyelonefritida), velké množství hlenu a masivní leukocyturie je příznakem infekce močových cest. Masivní leukocyturii označujeme jako hnis v moči (pyurie).
Epitelie
Pocházejí z epitelové výstelky renálních tubulů, z močového měchýře nebo z pohlavních orgánů.
- Epitelie renální tubulární – poměrně malé, kulovité nebo oválné útvary, ostře ohraničené, s velkým kulatým jádrem (zpravidla excentricky uloženým) bez jadérek, granulovanou protoplazmou, která často obsahuje světlo lámající tukové částice (zrníčka). Mezi epiteliemi jsou nejmenší.
+
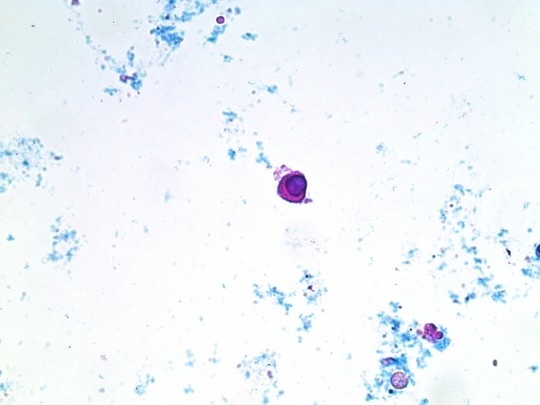
Zdroj: Autor Ing. Ivana Hupáková, Renální tubulární epitelie, licence Creative Commons BY-SA 4.0.
Obr. 24. Renální tubulární epitelie (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Vyskytují se buď jednotlivě, nebo jsou na sebe „taškovitě“ nakupeny či vytvářejí válce. Jsou jen o něco větší než leukocyty, za které mohou být zaměněny. Nález tohoto druhu epitelií je patologický, je známkou závažného poškození ledvin (silné poškození renálních tubulů např. při akutní tubulární nekróze, akutní intersticiální nefritidě, virové infekci, otravě těžkými kovy, nefrotoxickými léky aj.). Ostatní druhy epitelií se mohou vyskytnout i bez onemocnění ledvin.
- Epitelie přechodné – útvary se zrnitou protoplazmou, obsahující 1 – 2 jádra s malými světlolomnými tělísky. Mají různý tvar (většinou kulatý nebo okrouhlý, méně často vřetenovitý) a velikost dle jejich původu.
+
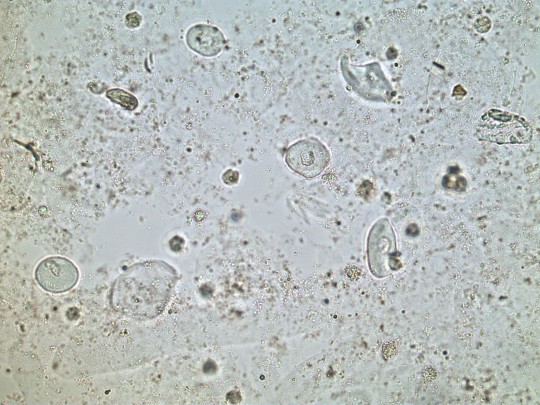
Zdroj: Autor Ing. Ivana Hupáková, Přechodné epitelie, licence Creative Commons BY-SA 4.0.
Obr. 25. Přechodné epitelie (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Pocházejí z močovodů, močového měchýře nebo proximální části uretry. Vyskytují se buď jednotlivě, nebo ve shlucích. Ojedinělý nález epitelií přechodných je fyziologický. Velké množství svědčí obvykle o infekci dolních močových cest (zvláště při současném výskytu leukocytů), může se také vyskytnout po katetrizaci a dalších invazivních zákrocích. Dvoujaderné buňky se nacházejí v moči pacientů s uroteliálními karcinomy nebo močovými konkrementy.
- Epitelie dlaždicové – největší buňky v močovém sedimentu, velké nepravidelné, s dobře viditelným malým jádrem uprostřed.
+
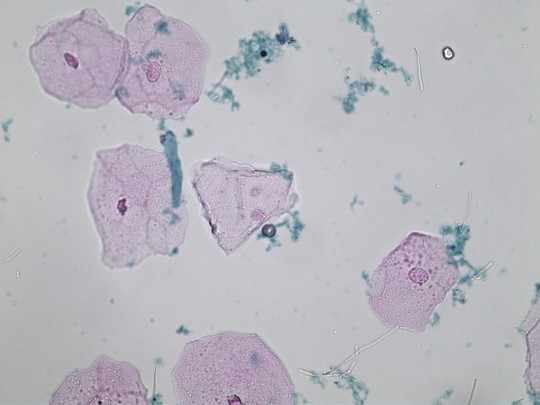
Zdroj: Autor Ing. Ivana Hupáková, Dlaždicové epitelie, licence Creative Commons BY-SA 4.0.
Obr. 26. Dlaždicové epitelie (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Pochází z vaginy a z dolní ⅓ močové trubice. Nemají klinický význam.
Močové válce
Hyalinní – bezbarvé nebo nažloutlé homogenní útvary různé délky, obvykle však krátké a rovné (mohou být i prohnuté a vzájemně vklíněné) se zaoblenými konci.
+
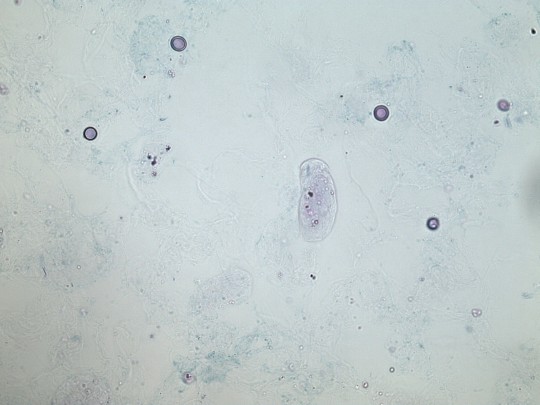
Zdroj: Autor Ing. Ivana Hupáková, Hyalinní válec a erytrocyty, licence Creative Commons BY-SA 4.0.
Obr. 27. Hyalinní válec a erytrocyty (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Mohou se vyskytnout po námaze, při horečce a u dehydratovaných osob. Obvykle neznamenají poškození ledvin.
Granulované – kratší a silnější než válce hyalinní, mají zrnitou strukturu. Nález většího počtu granulovaných válců je silně patologický, svědčí pro poškození tubulárních buněk.
+
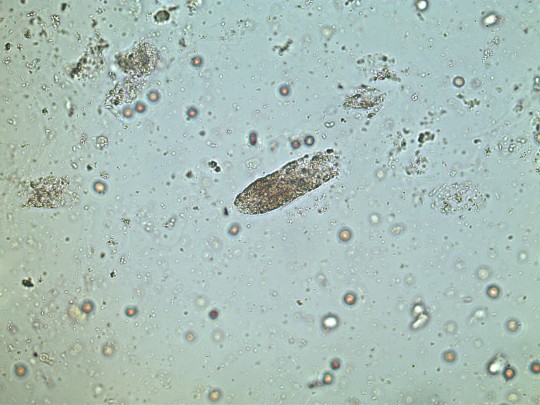
Zdroj: Autor Ing. Ivana Hupáková, Granulovaný válec nebarvený, licence Creative Commons BY-SA 4.0.
Obr. 28. Granulovaný válec nebarvený (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
+
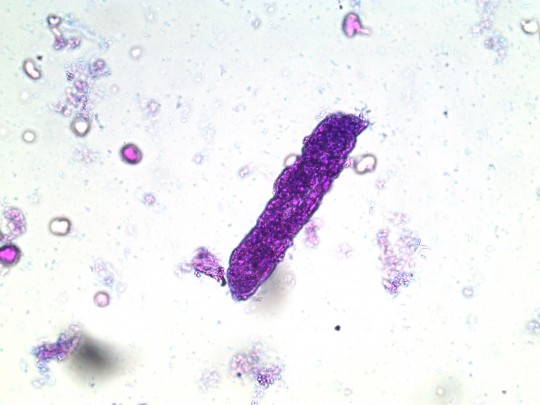
Zdroj: Autor Ing. Ivana Hupáková, Granulovaný válec barvený, licence Creative Commons BY-SA 4.0.
Obr. 29. Granulovaný válec barvený (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Voskové – tlustší než ostatní válce, mají voskový vzhled a často typické hluboké zářezy. Nálezy voskových válců patří k nejzávažnějším (tzv. válce renálního selhání).
Válce buněčné – rozlišujeme je podle buněk, z kterých jsou složeny, přičemž příslušné buňky musí tvořit alespoň 1/3 povrchu válce. Dělíme je na válce epiteliální, erytrocytární, leukocytární, bakteriální. Renální epiteliální válce jsou příznakem těžkého poškození tubulů.
+
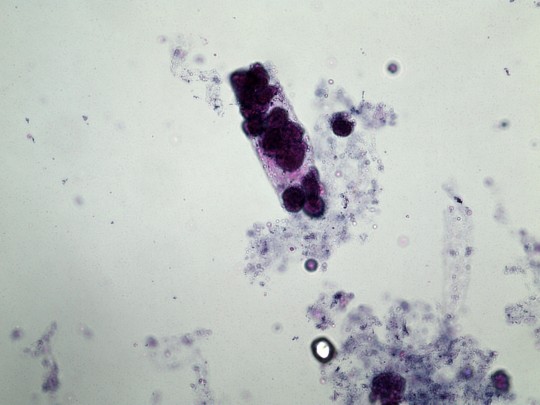
Zdroj: Autor Ing. Ivana Hupáková, Válec z renálních tubulárních epitelií, licence Creative Commons BY-SA 4.0.
Obr. 30. Válec z renálních tubulárních epitelií (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Erytrocytární válce jsou známkou glomerulonefritidy. Jsou extrémně křehké, brzy se rozpadají a jejich nález je proto velkou vzácností.
Leukocytární válce se vyskytují při zánětlivém onemocnění ledvin bakteriálního i nebakteriálního původu.
Nález bakteriálních válců je v současné době používání antibiotik velmi vzácný, neboť k jejich vzniku je nutná jednak silná bakteriurie a současně proteinurie.
Tukové válce obsahují kulatá tuková tělíska. Nacházejí se v moči při poškození glomerulů, u nefrotického syndromu, u diabetiků nebo po intoxikaci rtutí.
Pseudoválce – válcovité útvary anorganického i organického původu, nevznikají však v ledvinných kanálcích a nemají bílkovinný základ.
KRYSTALY A DALŠÍ SOUČÁSTI MOČOVÉHO SEDIMENTU
Nález krystalů v močovém sedimentu nemá, s výjimkou cystinu a častějšího nálezů tripelfosfátu při močových infekcích, příliš velký klinický význam.
Kyselina močová – vyskytuje se často v kyselé moči, tvoří tvarově různé (šestiboké, soudečkovité nebo vřeténkovité) krystaly, které mohou být spolu různě pospojovány do snopečkovitých nebo metličkovitých útvarů.
+

Zdroj: Autor Ing. Ivana Hupáková, Kyselina močová, licence Creative Commons BY-SA 4.0.
Obr. 31. Kyselina močová (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Amorfní drť – v kyselé moči se jedná převážně o kyselinu močovou a její soli (močany, uráty). Tvoří je malá amorfní zrníčka močanu draselného, vápenatého a hořečnatého, vyskytující se ve velkých shlucích. V alkalických močích se jedná o fosfáty – fosfátová drť.
+
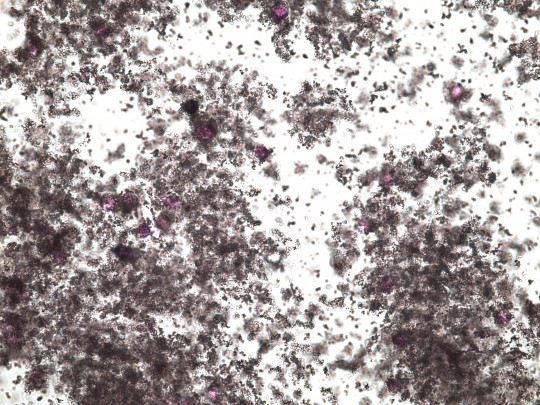
Zdroj: Autor Ing. Ivana Hupáková, Amorfní drť, licence Creative Commons BY-SA 4.0.
Obr. 32. Amorfní drť (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Močan amonný – tvoří kuličky s „ostnatými“ okraji („trnová jablka“). Je jedinou solí kyseliny močové, která se vyskytuje v slabě alkalické moči.
+
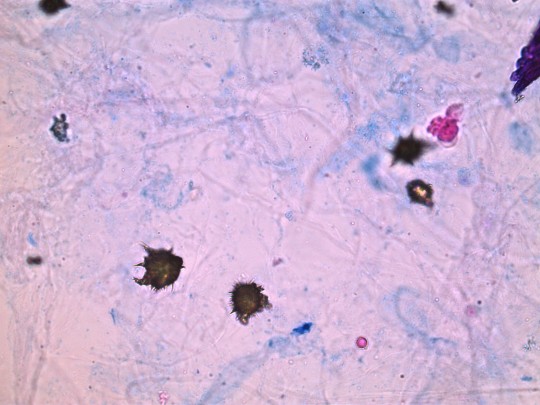
Zdroj: Autor Ing. Ivana Hupáková, Močan amonný, licence Creative Commons BY-SA 4.0.
Obr. 33. Močan amonný (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Fosforečnan amonnohořečnatý („tripelfosfát“) – vyskytuje se hlavně v alkalické moči v nejčastěji tzv. „rakvičkovité formě“, méně často ve formě připomínající tvarem vlaštovčí křídlo, peříčka, listy kapradí apod. Jde o velmi obvyklý nález v močích při infekci močových cest.
+
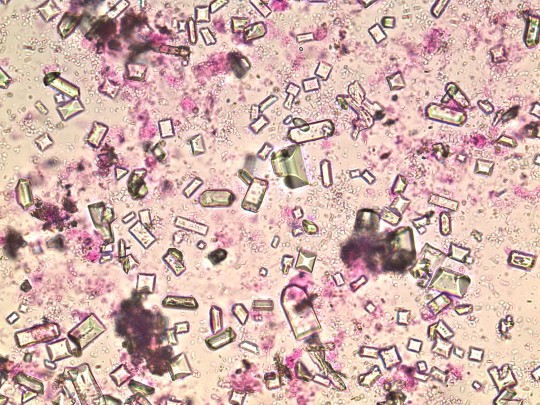
Zdroj: Autor Ing. Ivana Hupáková, Tripelfosfát, licence Creative Commons BY-SA 4.0.
Obr. 34. Tripelfosfát (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Neutrální fosforečnan hořečnatý – vyskytuje se zřídka a pouze v alkalických močích, ve formě velkých kosočtverečných destiček.
Šťavelan vápenatý (oxalát vápenatý) – vyskytuje se v kyselé, neutrální i slabě alkalické moči, nejčastěji ve formě pravidelných osmistěnů – „psaníček“ různých velikostí. Méně často tvoří čtyřboké hranoly s jehlany na obou koncích, kulaté tvary a krystaly tvaru činek (piškotů). Je charakteristickým nálezem u otravy ethylenglykolem. Vyskytuje se také v moči vegetariánů a veganů.
Síran vápenatý – se vyskytuje zřídka a pouze v silně kyselé moči, tvoří bezbarvé jehlice se šikmo ukončenými plochami, někdy bývají tyto krystaly sdružené do snopečků, hvězdicovitých útvarů nebo drúz.
Uhličitan vápenatý – vyskytuje se v zásadité, vzácněji v neutrální nebo slabě kyselé moči, krystaly mají tvar malých, šedých zrníček, obvykle uspořádaných do „činek“.
Leucin – tvoří kulovité, lesklé, žluté útvary koncentricky vrstvené, často příčně pruhované.
Tyrosin – tvoří lesklé jehlicovité krystaly, často spojené do metliček, snopečků, hvězdic nebo rozet.
Cystin – tvoří bezbarvé, světlo lámající pravidelné tenké šestiboké tabulky, často na sebe poskládané ve vrstvách.
Krystaly aminokyselin cystinu, leucinu, tyrosinu mají klinický význam u pacientů se specifickou aminoacidurií (cystinurie, leucinurie, tyrosinurie atd.).
Některé další součásti močového sedimentu:
V močovém sedimentu se dále mohou vyskytovat sekrety pohlavních žláz (spermie),
+
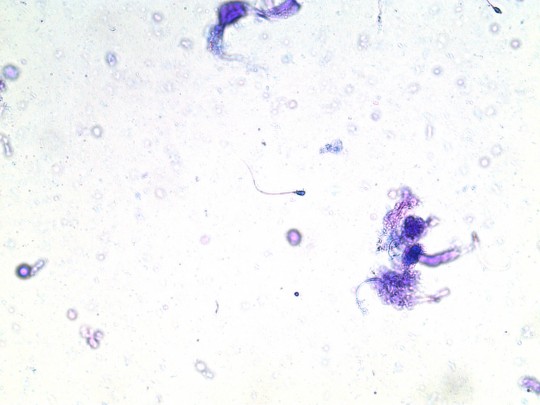
Zdroj: Autor Ing. Ivana Hupáková, Spermie, licence Creative Commons BY-SA 4.0.
Obr. 35. Spermie (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
hlen,
+
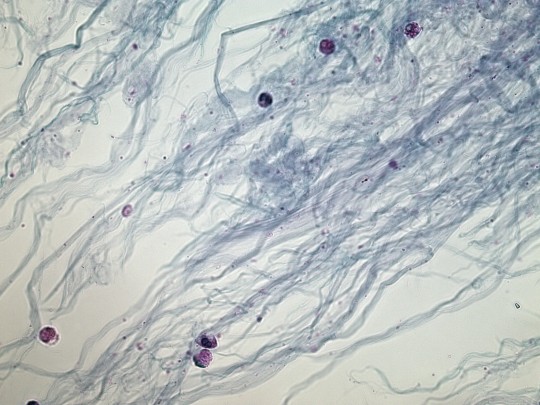
Zdroj: Autor Ing. Ivana Hupáková, Hlen a leukocyty, licence Creative Commons BY-SA 4.0.
Obr. 36. Hlen a leukocyty (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
bakterie,
+
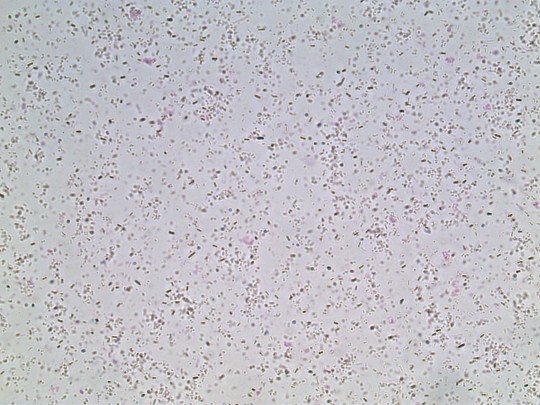
Zdroj: Autor Ing. Ivana Hupáková, Bakterie, licence Creative Commons BY-SA 4.0.
Obr. 37. Bakterie (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
Trichomonas vaginalis, kvasinky,
+
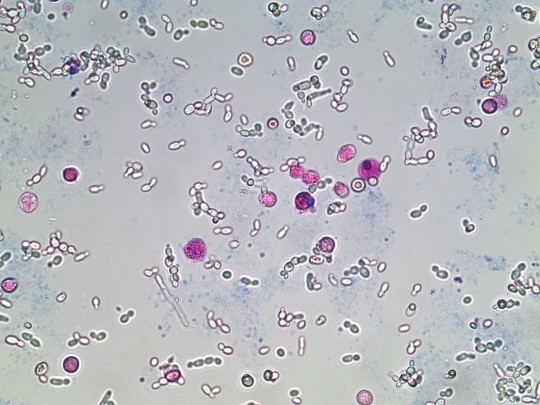
Zdroj: Autor Ing. Ivana Hupáková, Kvasinky, licence Creative Commons BY-SA 4.0.
Obr. 38. Kvasinky (foto Ing. Ivana Hupáková, ÚKBH Plzeň)
plísně a různé náhodné znečištěniny močového sedimentu (vlákna lnu, vlny, papíru, vlasy, rostlinná vlákna aj.)
V současné době se k morfologickému vyšetření močového sedimentu používají automatické analyzátory, založené buď na principu průtokové cytometrie nebo na principu digitálního snímání částic. Mikroskopické vyšetření močového sedimentu se provádí pouze u nejasných nebo rozporuplných nálezů.