Kapitola3
Farmakokinetické parametry, klinická farmakokinetika
Definice
Klinická farmakokinetika se zabývá vztahem mezi farmakologickou nebo toxickou odpovědí na léčivo a dosaženou koncentrací léčiva v plazmě nebo krvi. V mnohých případech je koncentrace léčiva v systémové cirkulaci v přímém vztahu ke koncentraci léčiva v místě účinku [2].
Důležitost farmakokinetiky v péči o pacienta spočívá ve zlepšení účinnosti léčby, jehož může být dosaženo tím, že budou brány v úvahu a dodržovány principy farmakokinetiky při stanovení modifikované dávky léčiva.
Různé fyziologické a patofyziologické proměnné veličiny mění farmakokinetické parametry a nutí k úpravě dávek u individuálních pacientů.
Mezi tři nejdůležitější farmakokinetické parametry patří:
- Clearance
- Distribuční objem
- Biologická dostupnost (frakce léčiva absorbovaného do systémové cirkulace) [2].
Definice
Clearance představuje objem biologické tekutiny (krev nebo plazma), který bude kompletně očištěn od léčiva za jednotku času. Celkové vyloučené množství látek je součtem všech druhů eliminace a je charakterizováno systémovou clearance. Clearance představuje eliminaci léčiva různými orgány (ledviny, játra, aj.) Clearance je důležitý farmakokinetický parametr, kterým lze postihnout dlouhodobé podávání léčiva [2].
Kinetika prvého řádu – za určitou časovou jednotku se vyloučí stejné množství látky aktuálně přítomné v organismu. Snadno zjistitelný parametr t1/2 → časový interval, za který klesá plazmatická koncentrace látky (a tedy i její přítomné množství) vždy na polovinu předchozí koncentrace. Z hodnoty t1/2 lze vypočítat eliminační konstantu k e= 0,693/t1/2 [2].
Rychlost eliminace látky je závislá na eliminační konstantě, která udává množství vyloučené látky z aktuálně přítomného množství látky v organismu. Má rozměr x/min, x/hod, např. 0,01/min, což ukazuje na vyloučení 1 % aktuálně přítomné látky za minutu [2].
Při eliminaci látek kinetikou nultého řádu (dosti vzácný případ), např. vylučování etanolu, je vyloučeno vždy konstantní množství látky, takže její koncentrace v plazmě klesá lineárně.
Clearance je konstantní, pokud je léčivo eliminováno kinetikou prvního řádu. Takto je eliminována většina terapeuticky používaných léčiv. Clearance je proměnlivá veličina, když je léčivo eliminováno kinetikou nultého řádu [2].
Distribuční objem
Definice
Distribuční objem je důležitý farmakokinetický kinetický parametr v posuzování procesu dispozice léčiv v organismu. Jedná se o poměr podané dávky a v plazmě naměřené koncentrace léčiva [2]. Distribuční objem je mírou kapacity distribučního prostoru látky.
V podstatě bychom mohli říci, že je to fiktivní objem tekutiny nutný k tomu, aby účinná látka byla v celém těle ve stejné koncentraci, jaká byla naměřena v krevní plazmě. Velké hodnoty distribučního objemu tak svědčí pro distribuci látky do intracelulárního prostoru [4]. Mnoho léčiv má distribuční objem mnohem větší, než jsou skutečné objemy tělesných tekutých kompartmentů. Např. objem digoxinu u 70 kg jedince, je Vd digoxinu u 70 kg jedince, je 700 l, což je mnohem větší objem, než činí u tohoto jedince objem celkové tělesné vody. Je to způsobeno tím, že digoxin je hydrofóbní látka, je distribuován odlišně do tukové tkáně, do svalů a k receptorům, v plazmě zůstává velmi malé množství [2].
U léčiv, která jsou silně vázána na plazmatický protein a nejsou vázána na tkáňové komponenty, se bude distribuční objem teoreticky blížit objemu plazmy.
Distribuční objem závisí:
- pKa léčiva,
- vazbě na bílkoviny plazmy,
- lipofilitě,
- stupni vazby na ostatní tkáně,
- věku pacienta,
- pohlaví,
- nemoci.
Definice
Distribuční objem v ustáleném stavu Vss – představuje objem, do kterého by bylo léčivo zdánlivě distribuováno během ustáleného stavu (steady state), vyskytuje-li se léčivo v tomto objemu ve stejné koncentraci jako v měřené tekutině (plazma nebo krev). Tento parametr není snadné stanovit [2].
3.1.1
Rozsah a rychlost absorpce léčiv, biologická dostupnost, bioekvivalence
Je nutné rozlišit: rychlost, rozsah absorpce a množství léčiva, které dosáhne systémové cirkulace.
Příklad
Např. k tomu, aby léčivo přešlo z kapiláry tenkého střeva do systémové cirkulace, nemusí jen penetrovat střevní sliznicí, může být atakováno počtem enzymů, které jej mohou inaktivovat jak ve střevě, tak v játrech.
Množství léčiva, které dosáhne systémové cirkulace, může být vyjádřeno jako frakce dávky (F) → biologická dostupnost (bioavailability). Biologická dostupnost beroucí v úvahu jak absorpci, tak lokální metabolickou degradaci, není jedinou charakteristikou pro lékový preparát, mění ji rozdíly v enzymové aktivitě střevní stěny nebo jater, žaludeční pH, střevní motilita.
Příklad
Např. je-li léčivo úplně absorbováno za 40 min, dosáhne mnohem většího vrcholu plazmatické koncentrace a následně i terapeutického účinku, než je-li absorbováno podstatně pomaleji. Proto u generických ekvivalentů patentovaných látek je kladen zásadní důraz na průkaznost bioekvivalence. Ta znamená, že nový produkt se chová dostatečně podobně jako standardní produkt a může jej nahradit, aniž by to způsobilo klinické problémy [2].
3.1.2
Vztah mezi dávkou, koncentrací a farmakologickým účinkem léčiv
U farmakokinetických modelů je plocha pod křivkou plazmatických koncentrací křivkou v závislosti na čase (AUC) přímo úměrná celkovému množství léčiva obsaženého v plazmatickém kompartmentu. Srovnání AUC po p.o. a i.v. aplikaci může být použito k určení biologické dostupnosti p.o. aplikovaného léčiva. Neúplná absorpce léčiva nebo rozklad při prvním průchodu játry dříve, než léčivo dosáhne plazmatického kompartmentu, budou znamenat, že AUC po p.o. aplikaci bude nižší než po aplikaci i.v., u níž uvedené děje nejsou ovlivněny rychlostí absorpce [2].
+
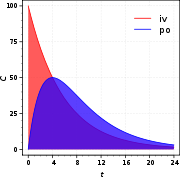
Obr. 7. Vztah koncentrace léčiva v plazmě po i.v. a p.o. aplikaci v závislosti na čase (AUC)
3.1.3
Terapeutické monitorování koncentrací léčiv a optimalizace dávkovacího režimu
U mnoha onemocnění je farmakoterapie úspěšná pouze tehdy, jestliže se koncentrace léčiva v krvi udržuje na dostatečné stabilní výši. Od pacienta se vyžaduje pravidelné užívání léčiva a takové dávkování, které nedovolí pokles pod terapeutickou koncentraci. U většiny klinických situací se léčiva aplikují ve formě opakovaných dávek, popř. jako kontinuální infúze, aby byla udržena ustálená koncentrace léčiva v plazmě v rozsahu daném terapeutickým rozmezím → intenzivní péče. Při perorálním podání se rozdělí celková denní dávka na několik jednotlivých (2-4) a následně plazmatická koncentrace léčiva mírně kolísá. Rozsah kolísání se může zmenšit, jestliže se podá retardovaná LF, z níž je léčivo uvolňováno pomaleji [2].
V některých případech je dlouhodobé udržování konstantní plazmatické koncentrace nežádoucí. Urychluje se ztráta účinnosti – rozvoj tolerance, návyku. Primárním cílem je výpočet vhodné udržovací dávky. Pro získání cílové hodnoty musí být rychlost podávání léčiva stejná jako rychlost jeho vylučování. Není vhodné kolísání koncentrací léčiva mezi jednotlivými dávkami. Pokud je léčivo relativně netoxické, pak mohou být snadněji tolerovány i koncentrace vyšší, než terapeutické. Dávkovací interval pak může být delší než poločas léčiva. Např. penicilin G má eliminační poločas menší než 1 hod, je proto podáván ve velmi vysokých dávkách, každých 6 hodin [2].
Pro některá léčiva s úzkým terapeutickým rozmezím (např. digoxin) je důležité určit maximální a minimální koncentrace, kterých by mělo být dosaženo při určitém dávkovacím intervalu. Někdy je nutné, aby se jednou dávkou popř. sérií dávek docílilo cílové koncentrace již na začátku terapie.
3.1.4
Iniciační, úvodní, nárazová dávka (loading)
Výpočet a zavedení nárazové dávky mohou být vhodné tehdy, je-li doba potřebná k dosažení ustálené koncentrace při aplikaci léčiva konstantní rychlostí příliš dlouhá s ohledem na účel léčby.
Příklad
Např. eliminační poločas lidokainu je delší než 1 hod. Arytmie doprovázející infarkt myokardu mohou být život ohrožující, nemůžeme čekat 5-6 hod, než se docílí terapeutické koncentrace lidokainu infúzí léčiva rychlostí nutnou k dosažení této koncentrace. Použití iniciační dávky je v kardiologické akutní péči zavedeno jako standard, dávky jsou podávány rychle, parenterálně.