2.1
Živné půdy
V mikrobiologických laboratořích jde především o zachování, oživení, pěstování, průkaz a/nebo stanovení počtu určovaných mikroorganismů. K tomuto účelu slouží kultivační půdy, které se využívají ve všech standardních i alternativních kultivačních technikách.
Kultivační stanovení jsou založeny na živných půdách, které poskytují neměnné a reprodukovatelné výsledky, proto všechny používané půdy musí vyhovovat stanoveným kritériím výkonnosti, které jsou předpokladem pro spolehlivou mikrobiologickou práci.
Definice
Jako živné půdy nazýváme materiály obsahující nepostradatelné a využitelné zdroje výživy a energie pro mikroorganismy. Musí vyhovovat všem nárokům příslušného mikroorganismu na výživu.
Definice
ČSN EN ISO 11133 Mikrobiologie potravin, krmiv a vody – Příprava, výroba, uchovávání a zkoušení výkonnosti kultivačních půd
Jedná se o mezinárodní normu, která definuje termíny týkající se zajišťování kvality kultivačních půd určených pro mikrobiologickou analýzu potravin, krmiv a vzorků z prostředí výroby potravin nebo krmiv a také všech druhů vody určených pro lidskou spotřebu nebo při výrobě potravin. Požadavky této normy platí nejen pro všechny kultivační půdy určené k mikrobiologickému zkoušení, ale i pro všechny kdo půdy připravují.
2.1.1
Rozdělení živných půd
Živné půdy lze dělit podle několika kritérií. Kvalita a volba vhodných živných půd je jedním z hlavních faktorů majících vliv na konečný výsledek kultivačního stanovení.
2.1.1.1
Podle původu
Syntetické půdy
Jedná se o živné půdy, které mají chemické složení přesně definováno. Většinou se jedná o ústojné roztoky, kde zdrojem uhlíku bývá glukóza, zdrojem dusíku (NH4)2SO4 nebo NH4Cl. Přidávají se některé vitamíny, aminokyseliny, biogenní prvky, růstové faktory.
Přirozené živné půdy
Jedná se o média, jejichž složení se nedá přesně definovat. Jsou komplexní a chemicky nedefinované. Hlavní složky se získávají hydrolýzou kaseinu, autolýzou nebo hydrolýzou pekařského droždí (extrakt z kvasinek – yeast extract), fermentativní hydrolýzou masa (masový výtažek – beef extract), působením žaludečních šťáv na rostlinné a živočišné bílkoviny (pepton). Tyto preparáty tvoří i část receptury univerzálních nebo speciálních bakteriologických půd. Do této skupiny patří také stanoviště mikroorganismů používaná v laboratořích např. brambory, mrkev, bílé pečivo, chleba, kroupy, žluč, apod.
Polopřirozené živné půdy
Meziskupina, která je kombinací přírodních surovin a přesně definovaných chemických látek. Základem je přírodní substrát doplněný přesně známým množstvím chemické látky (indikátory, soli, cukry, vitamíny, aminokyseliny, apod.), mají stálé vlastnosti. V praxi nejčastěji využívaná skupina živných půd.
2.1.1.2
Podle konzistence
Půdy tekuté
Jedná se o tekutá média ve formě vodného roztoku např. MPB (maso-peptonový bujón), sladina, mléko, živné roztoky, které slouží především pro pomnožení mikroorganismů. Růst mikrobiální kultury se projeví obvykle zákalem půdy, sedimentem, tvorbou kožky, usazeniny, prstence apod.
Obecně se tekuté půdy ve zkumavkách, baňkách nebo lahvích označují jako „bujóny“.
+

Obr. 1. Tekutá živná půda v baňce
+

Obr. 2. Tekutá živná půda ve zkumavce
Polotuhé (tuhé půdy)
Často se připravují přidáním agaru nebo jiného ztužovadla do bujónového základu. Jedná se tedy o tekutou půdu obsahující ztužovací látky v různých koncentracích. Používají se ke kultivaci mikroorganismů, k testování produkce některých metabolitů nebo enzymů.
Vzhledem k tomu, že nejčastěji se používají půdy ztužené agarem, vžil se termín „agar“ jako synonymum pro tuhé půdy. Tyto půdy rozplněné do Petriho misek se obecně označují jako „plotny“, rozplněné do zkumavek a ztuhlé v šikmé poloze se označují jako „šikmý agar“, pokud je půda rozplněna tak, že zaplní dno nádoby, vytvoří se „agarový sloupec“.
+

Obr. 3. Polotuhá živná půda agarová
Pevné půdy
Dovolují růst mikroorganismů v místě, na kterém byly naočkovány. Po inkubaci vyrůstá na povrchu tuhé půdy kolonie. Jedná se např. o plátky mrkve, jablka, brambory, kroupy, kostky chleba, rohlíku (vše sterilní).
2.1.1.3
Podle funkce
Půdy univerzální (kolektivní)
Svým složením vyhovují požadavkům na výživu širokého spektra mikroorganismů např. SA (sladinový agar), MPA (maso-peptonový agar), GTK (agar s glukózou, tryptonem a kvasničným extraktem).
Půdy selektivní
Jejich složení podporuje růst jednoho druhu nebo skupiny mikroorganismů. Růst doprovodné mikroflóry je inhibován. Složení odpovídá živnému základu s přídavkem inhibitoru růstu nežádoucích mikroorganismů (žlučové soli, antibiotika, krystalová violeť, nízké pH). Půdy mohou být tekuté i polotuhé např. VČŽL (půda s laktózou, krystalovou violetí, neutrální červení a žlučovými solemi), BGA (půda s laktózou, brilantovou zelení a fenolovou červení), GKCH (agar s glukózou, kvasničným extraktem, chloramfenikolem).
Půdy diagnostické
Určení daného mikroorganismu je založeno na jeho vybraných biochemických vlastnostech, které jsou podmíněny jeho enzymovou výbavou. Půda obsahuje živný základ, potřebný substrát (např. sacharidy, aminokyseliny, minerální látky, vitamíny) a indikátor biochemické aktivity (např. indikátor změny pH). Rozlišujeme půdy tekuté (např. cukrová média, půdy pro průkaz tvorby indolu) a polotuhé např. TSI (triple sugar iron agar).
Půdy selektivně diagnostické
Kombinují principy půd selektivních a diagnostických. Roste na nich jen velmi malá skupina mikroorganismů, nejčastěji se ze směsi mikroorganismů vyselektuje pouze hledaný druh a zároveň dochází k potlačení nežádoucí mikroflóry. Díky utilizaci přidaného substrátu rostou stanovované mikroorganismy v morfologicky výrazně odlišných koloniích. Např. EA (Endův agar), DXL (agar s xylózou, deoxycholátem a lysinem), MAC (MacConkey agar), MYP (mannitol, egg yolk, polymyxin B agar), SBA (Slanetz-Bartley agar).
Půdy pomnožovací
Jedná se o tekuté živné půdy sloužící k pomnožení mikroorganismů tam, kde jsou přítomny v malém množství (např. selenitová půda pro pomnožení salmonel), aby se zvýšila záchytnost stanovení.
Půdy transportní
Využívají se v klinické mikrobiologii a slouží k zajištění přežití bakterií během transportu do laboratoře. Slouží tedy především ke konzervaci a zachování životaschopnosti mikroorganismů s podmínkou minimalizace změn jejich počtu. Jsou obvykle komerčně připraveny ve zkumavkách.
Půdy se sníženým redox-potenciálem
Využívají se pro kultivaci anaerobních bakterií. Snížení redoxního potenciálu dosáhneme přidáním redukujících látek do půd (např. cystein, thiosloučeniny).
Půdy chromogenní a fluorogenní
Představují zvláštní skupinu diagnostických půd. Chromogenní půdy obsahují substrát, který je zcela specifický k danému mikroorganismu, pro který je půda určena. Mikroorganismus umí substrát svým metabolismem zpracovat a výsledkem jsou jasně morfologicky identifikovatelné kolonie (např. pro průkaz salmonel, Listeria monocytogenes, Escherichia coli O157, enterokoků atd.). U půd fluorogenních je na substrát navázáno fluorescenční barvivo, kolonie se dokazují v UV světle při 360 nm typickou fluorescencí. Půdy jsou určeny pro rychlou detekci a kvantifikaci patogenních mikroorganismů nebo pro stanovení bakterií indikujících kvalitu výrobků nebo např. při stanovení E. coli v pitné vodě.
2.1.2
Složení živných půd
Živná půda představuje různě definovanou směs látek, která obsahuje přírodní i syntetické složky určené k pomnožení nebo zachování životaschopnosti mikroorganismů.
2.1.2.1
Voda
Voda je nepostradatelná pro život, její dostatečné množství umožní průběh životních pochodů. Pro přípravu se používá nejčastěji destilovaná voda, nelze použít vodu s vysokým obsahem solí, kovů, chloridů, CO2 apod.
2.1.2.2
Zdroje uhlíku
Mezi základní a nejčastěji používané zdroje uhlíku patří cukry (monosacharidy, disacharidy, polysacharidy), bílkoviny, organické kyseliny, alkoholy (glycerol, mannitol, sorbitol), přirozené látky (masový, sladový nebo kvasničný extrakt, pepton, hydrolyzáty kaseinu apod.).
2.1.2.3
Zdroje dusíku
Dusík je součástí řady nepostradatelných složek organismu. Mezi nejčastější zdroje dusíku patří organické zdroje jako aminokyseliny, peptidy, bílkoviny a jejich hydrolyzáty a přirozené látky. Mikroorganismy jsou schopné využívat i anorganické zdroje dusíku jako NH4+, NO3-.
2.1.2.4
Růstové faktory
Jedná se zejména o esenciální aminokyseliny, mastné kyseliny, vitamíny, soli organických a anorganických látek, nukleotidy apod., často obsažené v přirozených látkách.
2.1.2.5
Ostatní látky
Mezi ostatní látky se řadí např. specifické faktory (tributyrin, beraní krev apod.), indikátory (bromthymolová modř, neutrální červeň, TTC (triphenyltetrazolium chlorid) apod.), inhibitory (žlučové soli, chloramfenikol apod.), které umožňují růst, potlačení nebo detekci mikroorganismů.
2.1.2.6
Ztužovadla
Jedná se o součásti polotuhých živných půd. Vhodným záhřevem se mění jejich skupenství z gelu na sol, dochází tedy k ztekucení. Po ochladnutí dochází ke zpětnému procesu a ke ztuhnutí do původní konzistence. V mikrobiologii jsou nejčastěji využívané ztužovadla agar (označován jako agar-agar) a želatina. Při kultivaci autotrofních mikroorganismů, které jsou náchylné na přítomnost organických sloučenin, se jako ztužovalo, používá gel kyseliny křemičité.
Agar
Rostlinný polysacharid s velkou gelotvornou schopností, který se vyrábí z mořských řas. Jedná se o červené řasy rodů Floridae a Gelidium. Teplota tání je 96 °C a teplota tuhnutí 40 °C, dávka používaná pro přípravu živných půd se řídí podle receptury, nejčastěji bývá v rozmezí 1,5 – 3 %. Není živinou pro mikroorganismy, opakovaným záhřevem snižuje svou rosolovací schopnost.
+

Obr. 4. Agar
+

Obr. 5. Komerčně vyráběný agar
Želatina
Jedná se o směs živočišných bílkovin (kolagen, osein, chondrogen) pocházejících z kostí, kůže, chrupavek. Teplota tání je nad 25 °C a k úplnému ztekucení dochází již kolem 30 °C, což je velkou nevýhodou, teplota tuhnutí je 25 °C. Dávka používaná na přípravu živných půd se řídí dle receptury, nejčastěji bývá 10 – 20 %. Želatina je rozkládána proteolytickými mikroorganismy (dochází ke ztekucování želatiny – důkaz přítomnosti proteáz), opakovaným záhřevem snižuje svou rosolovací schopnost.
+

Obr. 6. Želatina plátek
+

Obr. 7. Želatina
+

Obr. 8. Komerčně vyráběná želatina
Vlastnosti a chemické složení želatiny a agaru
Želatina | Agar | |
Původ | Živočišný, z kostí, kůží, … | Rostlinný, z mořských řas |
Chemická povaha | Bílkovina | Polysacharid |
Reakce | Kyselá | Slabě kyselá |
Přídavek do tekutých půd | 10 – 20 % | 1 – 3 % |
Teplota tání | 25 °C | 96 °C |
Teplota tuhnutí | 25 °C | 40 °C |
Kondenzační voda | Žádná | Přítomna |
Proteolytické rozpouštění | Nastává | Nenastává |
Voda | 14 až 15 % | 16 % |
Popel | 0,6 % | 4,4 % |
CaO | - | 1,1 % |
MgO | - | 0,7 % |
N | 18,3 % | 0,4 % |
2.1.3
Příprava živných půd
V mikrobiologické laboratoři se můžeme setkat s půdami určenými k přímému použití, které jsou výrobcem dodávány ve formě již hotových živných půd v Petriho miskách, zásobních lahvích určených k rozvaření a vylití do Petriho misek nebo ve zkumavkách. Další možností je příprava živných médií přímo v laboratoři z komerčně vyráběných dehydratovaných směsí nebo z jednotlivých složek podle receptury. Klasická příprava médií spočívá ve využití složek jako např. bujónu, masového extraktu, peptonu, kvasniční vody, kvasničného extraktu, mléka, krve, žlučových derivátů, ostatních látek, ztužovadel apod. nebo v použití kompletní dehydratované půdy.
+

Obr. 9. Hotové živné půdy v Petriho miskách
+

Obr. 10. Hotové živné půdy v zásobních lahvích
2.1.3.1
Příprava komerčních dehydratovaných živných půd
Hotová dehydratovaná média se obvykle dodávají v podobě prášku, granulí, případně tablet. Balení obsahující komerčně vyráběné jednotlivé složky živných půd nebo kompletní půdy musí být skladovány podle pokynů výrobce v suchu, temnu, při teplotě uváděné výrobcem nebo při běžné laboratorní teplotě. Dehydratované materiály jsou hygroskopické, proto vždy pracujeme rychle a pečlivě uzavíráme obaly. Pokud půdy jeví známky změny vzhledu, tuhnutí, slepení, nebo pokud došlo k vypršení doby expirace uvedené výrobcem, není vhodné je dále používat.
Při manipulaci s dehydratovanými půdami a jinými složkami je důležité dodržovat správnou laboratorní praxi a pokyny uvedené výrobcem. Jedná se hlavně o půdy, které obsahují nebezpečné látky, např. žlučové soli, azid sodný, antibiotika nebo jiná selektivní činidla.
2.1.3.2
Postup přípravy živných půd
Voda
K přípravě živných půd z přírodního materiálu se většinou používá vodovodní voda (neměla by být příliš tvrdá, nevhodné je i větší množství železa a chloridů).
K rehydrataci komerčních půd se používá pouze purifikovaná voda, tj. destilovaná, demineralizovaná, deionizovaná nebo připravená reverzní osmózou. Tato voda se musí uchovávat v nádobách vyrobených z inertního materiálu, které neuvolňují žádné rezidua, nebo se doporučuje používat vodu ihned po přípravě. Mikrobiální kontaminace této vody nemá přesáhnout 103 KTJ (kolonie tvořící jednotky)/ml a má se pravidelně kontrolovat.
Vážení a rozpouštění
Podle receptury uvedené výrobcem nebo v příslušné normě se potřebné množství dehydratované půdy naváží s přesností 0,01 g a převede do vhodné nádoby. Její objem má odpovídat dvojnásobku připravovaného objemu živné půdy. Není-li uvedeno jinak, nedoplňuje se objem získané směsi do finální hodnoty, ale složky se přidají do stanoveného objemu vody.
Po nalití vody je vhodné důkladné promíchání živné půdy, tak aby nevznikly slepence u dna nádoby, které by znesnadňovaly rozpouštění. Pro zkrácení doby rozpouštění je vhodné agarové půdy nechat asi 15 minut bobtnat. Po nabobtnání se směs dobře promíchá a rozpouští ve vroucí vodní lázni nebo proudící páře, nejčastěji v Kochově hrnci. Ohřev v mikrovlnné troubě není příliš vhodný, často dochází k místnímu přehřátí. Obsah průběžně promícháváme, aby nedošlo k sedimentaci částic na dno nádoby. Po dokonalém a šetrném rozpuštění, kdy na stěnách nejsou viditelné částice agaru (agarové slzy) se médium vychladí a provede se měření a úprava pH na hodnotu stanovenou normou či výrobcem.
Měření a úprava pH
K měření pH použijeme pH metr nebo indikátorové papírky pH. Hodnota se upraví tak, aby po sterilaci a ochlazení na 25 °C půda dosáhla požadované hodnoty s tolerancí ±0,2 jednotky pH. K úpravě pH se používá roztok NaOH o koncentraci 1 mol/l, což odpovídá koncentraci 40 g/l, nebo zředěná HCl o koncentraci 1 mol/l, což odpovídá přibližně koncentraci 36,5 g/l.
Při úpravě pH musíme brát v úvahu, že sterilizací v autoklávu hodnota poklesne o 0,1 – 0,2. Z tohoto důvodu lze úpravu pH provádět až po sterilizaci, nesmí však dojít ke kontaminaci již sterilního živného média a musíme používat vysterilizované roztoky.
Bakterie vyžadují nejčastěji pH 7 – 7,3. Kvasinky a plísně vyžadují pH v rozmezí 4,5 – 6,0. Konkrétní pH pro danou živnou půdu je vždy uvedeno v receptuře.
+
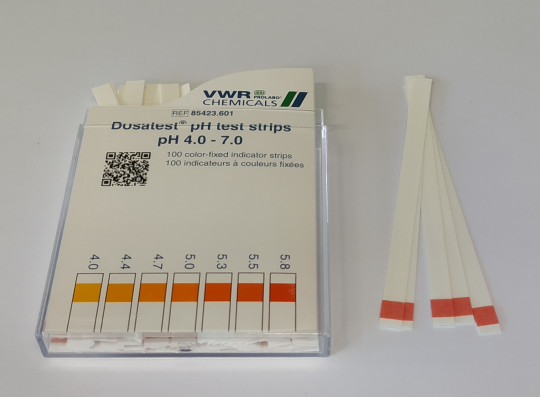
Obr. 11. Indikátorové papírky
+
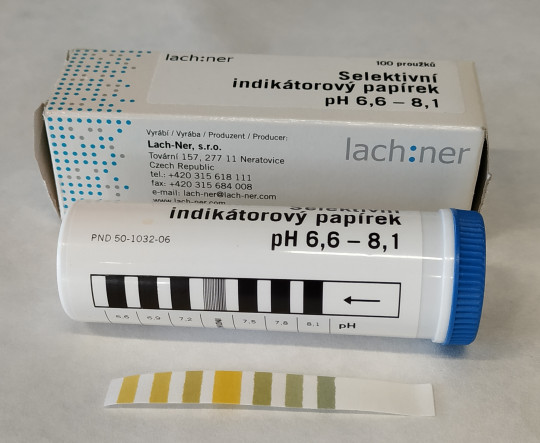
Obr. 12. Indikátorové papírky
2.1.3.3
Sterilizace půd
Definice
Sterilizace znamená zneškodnění všech živých mikroorganismů v daném prostředí (objektu, látce, roztoku), které pak označujeme jako sterilní.
Živné půdy lze sterilizovat autoklávováním, frakcionovanou sterilizací nebo filtrací. Některé druhy půd se nesterilizují, ale pouze rozvářejí (např. SBA, VČŽL), podobně některé složky lze použít přímo bez sterilizace. Živné půdy se sterilizují ve vhodných nádobách nebo po rozplnění do zkumavek.
Sterilizace autoklávováním se provádí v autoklávu 15 – 20 minut při 121 °C za přetlaku 0,15 MPa. Jedná se o čistý čas sterilizace, do této doby se nepočítá čas nutný k docílení teploty 121 °C a následné zchlazení. Při sterilizaci větších objemů než 1 000 ml nebo při použití tlustostěnného skla se sterilizační doba upraví dle potřeby na 30 – 60 minut, ale vždy se musí brát v úvahu možnost přehřátí půdy s následným poklesem její gelotvorné schopnosti.
V případě, že hrozí poškození půdy nebo jejich složek vysokou teplotou při tlakové sterilizaci (želatinová média, mléko, půdy s vyšším obsahem cukru), sterilizujeme je tzv. frakcionovanou (přerušovanou) sterilací. Média zahříváme v proudící páře při atmosférickém tlaku za teploty 99 – 100 °C po dobu 20 – 30 minut. Postup opakujeme ve třech po sobě jdoucích dnech. Mezi jednotlivými záhřevy dochází k vyklíčení bakteriálních spor při pokojové teplotě během 24 hodin.
Živné půdy nebo roztoky lze také sterilizovat membránovou filtrací za podmínek vakua nebo přetlaku. Používají se membránové filtry s póry vhodnými pro mikrobiologickou filtraci, nejčastěji o průměru 0,22 μm a sterilní filtrační zařízení. Některé membránové filtry mohou zadržovat bílkoviny, nebo jiné látky (např. antibiotika). Proto, aby se udržela správná koncentrace látek v živné půdě, je nutné vybrat vhodný typ filtru.
2.1.3.4
Rozlévání živných půd a jejich uchovávání
Vysterilované živné půdy jsou po vychladnutí buď přímo připraveny k naočkování, nebo je třeba „rozplnit“ je do prázdných sterilních kultivačních nádob. Všechny operace spojené s otvíráním nádob je třeba provádět podle všech zásad aseptické práce, tj. se zamezením vniknutí kontaminace z nesterilního okolí. Nejčastěji provádíme tzv. lití ploten (nalévání živných půd do Petriho misek), přípravu vysokých sloupců a přípravu šikmých agarů.
Při rozlévání nesmí půda potřísnit okraje nádob ani vatové zátky, aby nedocházelo ke kontaminaci média mikroorganismy pomnoženými na zátkách.
+

Obr. 13. Šikmý agar, sloupec živné půdy
+
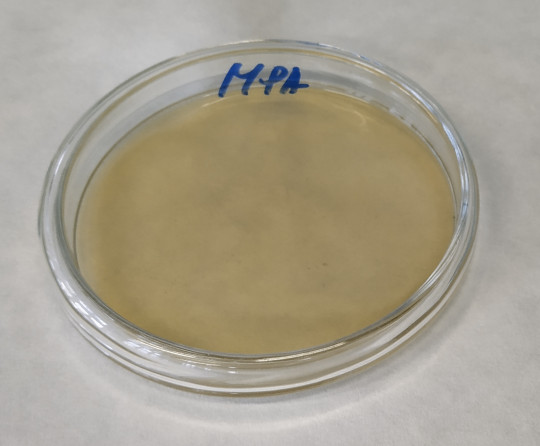
Obr. 14. Petriho miska s živnou půdou
Lití ploten
Vysterilovanou, rozehřátou a mírně ochlazenou agarovou nebo želatinovou půdu vyléváme z baněk nebo ze zkumavek do sterilních Petriho misek. Opatrně zdvihneme víčko Petriho misky a rychle vylijeme potřebné množství živné půdy, aby byla plocha misky pokryta do výše 3 – 5 mm. Pro misky o průměru 9 cm je třeba 15 – 20 ml živné půdy. Musíme dbát, aby okraj misky zůstal suchý. Misku ihned po nalití uzavřeme, ožehneme hrdlo i zátku baňky a uzavřeme. Nalité Petriho misky necháme ztuhnout ve vodorovné poloze. Po utuhnutí se agarové plotny použijí, nebo se uchovávají dnem vzhůru za podmínek, které brání zhoršení jejich kvality a dehydrataci, tj. v temnu a chladu. Nejlépe při (5 ±3) °C.
Lití půdy na šikmé agary
Sterilní rozehřátou agarovou nebo želatinovou půdu nalijeme do širších mikrobiologických zkumavek, nejvýše do jedné třetiny. Po sterilaci položíme zkumavky do speciálních stojánků, ve kterých živná půda ztuhne v šikmé poloze. Konec živné půdy má sahat asi do dvou třetin zkumavky. Živná půda nesmí nikdy ulpět na hrdle zkumavky nebo na vatové zátce. Šikmé agarové a želatinové půdy připravujeme vždy čerstvé. V zásobě můžeme mít zkumavky s půdou, ale ne šikmou. Tyto zkumavky pak podle potřeby rozehřejeme a necháme ztuhnout v příslušné šikmé poloze.
2.1.3.5
Příprava živných půd pro použití
Rozehřívání agarových kultivačních půd
Živné půdy se rozehřívají ve vroucí vodní lázni, např. v Kochově hrnci. Půdy, které prošly autoklávováním, se mají zahřívat co nejkratší dobu, aby nedošlo k přehřátí a zůstala zachována jejich kvalita. Uzávěry nádob se mají před ohřevem povolit a po jeho ukončení opět přitáhnout.
Rozehřátá půda se schladí ve vodní lázni na teplotu 47 – 50 °C a má se co nejdříve použít. Půdy určené pro očkování přelivem se vytemperují na 44 – 47 °C. Obecně platí, že se půda v tomto stavu nemá uchovávat déle než 4 hodiny. Nepoužitá půda se nesmí nechat znovu utuhnout a opakovaně používat.
Vypuzení vzduchu
Pokud je nutné zajistit správný obsah vzduchu, temperuje se půda těsně před použitím ve vroucí vodní lázni po dobu 15 minut. Víčka nebo uzávěry musí být povoleny, aby došlo k úniku vzduchu. Po ukončení záhřevu se uzávěry opět těsně uzavřou a půda se rychle ochladí na pracovní teplotu.
Přidávání suplementů
K některým půdám se musejí před rozplněním nebo jejich použitím přidávat tzv. suplementy (např. antibiotika, vaječný žloutek, beraní krev, některé chemické látky). Většinou se jedná o látky termolabilní, u nichž by došlo sterilizací k jejich znehodnocení.
Živná půda se před přidáním suplementů ochladí pod 50 °C. Suplementy, které uchováváme při nízkých teplotách nebo ve větším množství je vhodné před vlastním přidáním vytemperovat alespoň na pokojovou teplotu. Přidání studených tekutých suplementů může způsobit gelovatění agaru nebo tvorbu průsvitných vloček. Je potřeba dodržovat pokyny výrobce. Po přidání suplementu je nutné živnou půdu opatrně, ale řádně promíchat a následně co nejrychleji rozplnit do sterilních Petriho misek nebo zkumavek.
+
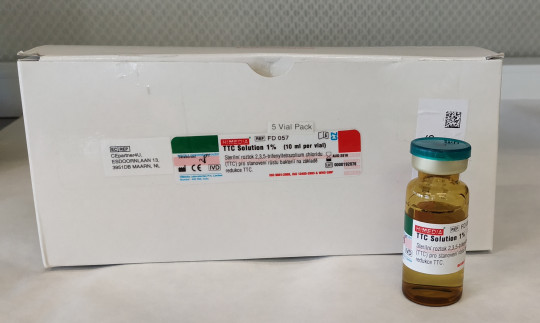
Obr. 15. Suplement
Příprava plotnových půd pro inokulaci
Pro očkování na povrch tuhých kultivačních půd se plotny krátce před použitím předsoušejí, přitom se musí dávat pozor, aby se nepřesušily. Při rozhodování o předsoušení se musí brát v úvahu několik aspektů:
- Stupeň vlhkosti v kultivačních půdách – značná ztráta vlhkosti může vést např. ke zvýšení koncentrace inhibitorů v selektivních kultivačních půdách a ke snížení vodní aktivity na povrchu půdy a tím k omezení růstu mikroorganismů.
- V případě kultivace nerozrůstajících se bakterií – kdy plotny vypadají po aklimatizaci při pokojové teplotě jako suché, není předsoušení nutné.
- Teplota a doba předsoušení se volí tak, aby se co nejvíce omezila možnost kontaminace.
- Aby se zabránilo kontaminaci, pokud se plotny předsoušejí mimo laminární boxy, musí se předsoušet otočené dnem vzhůru.
Misky se mohou předsoušet v sušárně při teplotě 25 – 50 °C s částečně sejmutými víčky a dnem vzhůru. Doba předsoušení je daná vymizením kapek vody z povrchu půdy. Pokud plotny předsoušíme v bezpečnostním boxu s laminárním proděním vzduchu (při pokojové teplotě), misky jsou otevřené a orientované povrchem agarové půdy nahoru, doba předsoušení je 30 – 60 minut.
Příklad
Úkol: Příprava polotuhých a tekutých živných půd.
Pomůcky: laboratorní sklo, váhy, pH papírky, destilovaná voda, roztoky na úpravu pH, zátky, alobalové krytky, jmenovky, živné půdy.
Postup:
- Připravte si pracovní místo a všechny pomůcky, které budete potřebovat.
- Do laboratorního deníku si zaznamenejte složení živné půdy, kterou budete připravovat, proveďte přepočet na požadované množství živné půdy (původní receptura je na 1 000 ml).
- Postupujte podle pokynů výrobce uvedeného na obalu nebo podle použité receptury.
- Dehydratovanou živnou půdu navažte s přesností 0,01 g do nádoby 2x větší než požadovaný objem.
- Navážku rozpusťte v destilované vodě a nechejte 15 minut nabobtnat. Poté zahřívejte v Kochově hrnci nebo ve vodní lázni až do úplného rozpuštění (čirá živná půda).
- Po rozpuštění a vychlazení živné půdy proveďte úpravu pH na požadovanou hodnotu podle receptury.
- pH zkontrolujte indikátorovými papírky, pro zvýšení pH použijte 0,1 M NaOH, pro snížení pH použijte 0,1 M HCl.
- Pokud to bude nutné (zákal) přefiltrujte živnou půdu přes papírové filtry v Büchnerově nálevce pomocí vývěvy.
- Živnou půdu rozplňte ke sterilaci podle použití.
- Tekuté půdy: zkumavky se zátkami, plynovky, vkládání do kovových košů.
- Polotuhé půdy: ještě za tepla se plní do varných nebo Erlenmayerových baněk, objem cca 200 ml, opatřit vatovou zátkou, hliníkovou folií, štítkem, nebo nalít do zkumavek a po vysterilizování nechat utuhnout vysoký sloupec nebo v šikmé poloze.
- Připravené živné půdy sterilizujte v autoklávu, pokud to půda vyžaduje, sterilizujte frakcionovaně v Kochově hrnci.
- Živné půdy uchovávejte v temnu v chladničce při (5 ±3) °C.
Hodnocení:
Zpracujte protokol z daného cvičení.
Závěr:
Zhodnoťte úspěšnost práce mezi skupinami.