5.2
První věta termodynamiky
5.2.1
Objemová práce
Problematika práce a tepla je klíčem k první termodynamické větě. Práce a teplo jsou dvě různé formy výměny energie mezi soustavou a okolím.
Objemová práce W plynu nastane při změně objemu z hodnoty V1 na hodnotu V2. K odvození použijeme představu válce, ve kterém je stlačován plyn.
+
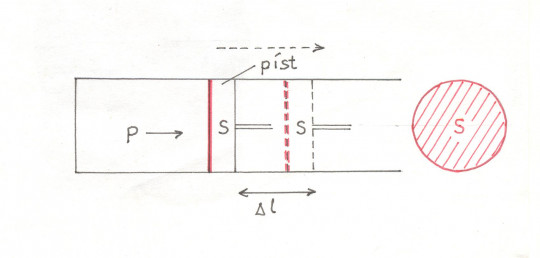
Obr. 24. Objemová práce – expanze plynu po stlačení pístem ve válci
Na obrázku je nakreslen válec s plynem. Plyn je stlačován pomocí pístu, dochází ke kompresi plynu. Po uvolnění pístu dochází k expanzi plynu. Plyn koná objemovou práci W. Plyn působí na plochu pístu S tlakem p. Celková síla působící na píst je F = p ∙ S. Píst se posune (směr posunu pístu je označen šipkou čárkovaně) o dráhový rozdíl ∆l:
Pokud je třeba vyjádřit, zda soustava přijala nebo vydala práci, pak konaná (vydaná) práce se značí záporným znaménkem a přijatá kladným.
5.2.2
Vnitřní energie
U termodynamického systému rozlišujeme vnější a vnitřní energii. Vnější energií myslíme u soustavy jako celku (např. tělesa) energii kinetickou (tj. pohybovou) a energii potenciální (tj. polohovou), kterou má každé těleso nacházející se v potenciálovém poli určité síly (např. v tíhovém poli).
V termodynamice nás ale zajímá vnitřní energie. Jedná se o souhrn různých energií částic a atomů v soustavě. Zahrnuje energii tepelnou (kinetickou energii elementárních částic), chemickou (vazebnou energii atomů v molekulách), jadernou (vazebnou energii nukleonů v jádrech atomů), polohovou (projevující se např. jako stlačitelnost/pružnost), popř. magnetickou, elektrickou. Vnitřní energii nelze v určitém okamžiku změřit. Je možné změřit pouze změnu vnitřní energie
, přechází-li soustava ze stavu A do stavu B.
Podle prvního termodynamického zákona platí:
Definice
První termodynamický zákon: Změna vnitřní energie soustavy ΔU se rovná součtu tepla Q a práce W vyměněné s okolím.
Jeden ze základních zákonů ve fyzice je zákon o zachování energie, který říká, že energie nemůže z ničeho vzniknout a také že ji nelze zničit, pouze ji lze přeměnit na jiný druh energie.
První věta termodynamiky je jeho specifickou formulací, podle níž teplo dodané systému může být přeměněno na práci nebo se spotřebovat na zvýšení obsahu vnitřní energie, popř. obojí současně.
Pozor:
Teplo a práce vyměněné mezi systémem a okolím při přechodu systému ze stavu A do stavu B závisejí nejen na uvedeném počátečním a konečném stavu, ale také na zvolené cestě mezi stavem A a B.
Součet tepla a práce je dán rozdílem
, tj. závisí pouze na počátečním a konečném stavu.
Poznámka
Matematická formulace I. věty termodynamické pro uzavřený systém zapsaná v diferenciálním stavu:
.
Symboly d a đ velmi zjednodušeně znamenají infinitezimálně malé změny. Písmeno d značí úplný diferenciál. Integrál úplného diferenciálu nezávisí na cestě. Symbol đ představuje neúplný diferenciál, jehož integrál závisí na cestě.
Integrál se v matematice používá např. k výpočtu plochy.
[infinitezimální = nekonečně malý, např. číslo]
Příklad
Příklad 5.1
Uzavřenému systému byla dodána energie 1200 J ve formě tepla. Jak se změnila vnitřní energie systému, jestliže vykonal práci 500 J?
Zobrazit řešení
Skrýt řešení
Řešení
ze zadání:
ΔU = ?
Q = 1200 J
W =
500 J (znaménko minus značí vykonanou práci)
výpočet:
Změna vnitřní energie je 700 J.
Příklad
Příklad 5.2
Soustava vykonala práci 58 kJ. Její vnitřní energie vzrostla o 12 500 J. Kolik tepla soustava přijala nebo odevzdala?
Zobrazit řešení
Skrýt řešení
Řešení
Q = + 70 500 J (+ značí soustavou přijaté, soustavě dodané)
Soustava přijala 70,5 kJ tepla.
5.2.3
Důsledky 1. zákona termodynamiky
Jestliže pro 1. zákon termodynamiky platí:
,
pak pro konanou práci musí platit:
Z rovnice je vidět, že soustava může konat práci na úkor úbytku vnitřní energie nebo na úkor dodaného tepla. Práce tedy nevzniká z ničeho.
Z prvního zákona termodynamiky vyplývá, že nelze sestrojit perpetuum mobile prvního druhu, tj. stroje, který by konal cyklicky práci, a přitom by nepřijímal z okolí energii. Stroj by se měl podle představy rozeběhnout nějakým počátečním impulsem a pak už by měl nepřetržitě běžet, aniž by mu byl dodáván jakýkoliv druh energie. Jinak řečeno, konal by užitečnou práci z ničeho.
První zákon termodynamiky ale nezakazuje přeměnit tepelnému stroji veškeré teplo v práci. Při matematickém odvozování nastane u cyklického děje, kde
. V kapitole o druhém termodynamickém zákoně se dozvíme, že to možné není.
Poznámka
Historické návrhy perpetua mobile často spočívaly v nedůsledném rozmyšlení rozložení sil v klasické mechanice. Jiné návrhy z této skupiny používají magnety jako nevyčerpatelný zdroj energie a vyhýbají se vzájemnému dotyku jednotlivých pohyblivých částí. Takové stroje často dokážou pracovat velmi dlouho. Problém je v tom, že ve skutečnosti nejsou schopny poskytnout žádnou skutečnou mechanickou práci k pohonu nějakého vnějšího zařízení. [57]
5.2.4
Změny vnitřní energie u jednotlivých dějů:
5.2.4.1
Izotermický děj, t = konst.
Vnitřní energie ideálního plynu je rovna energii pohybujících se molekul, která je funkcí teploty. Proto při konstantní teplotě bude změna vnitřní energie rovna nule.
Po dosazení:
Z matematického odvození plyne, že přijaté teplo se rovná vykonané práci a naopak odevzdané teplo se rovná přijaté práci.
Velikost práce závisí na cestě, proto budeme rozlišovat vratné a nevratné provedení expanze a komprese.
Izotermická expanze
+
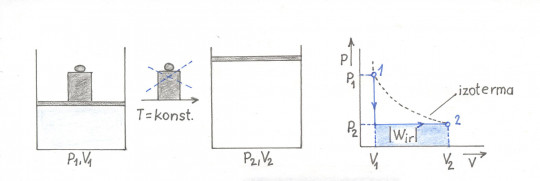
Obr. 25. Izotermická expanze – nevratná
+
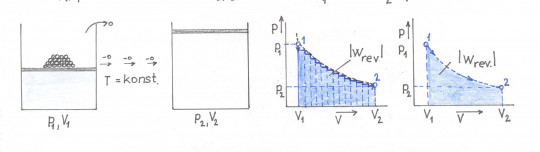
Obr. 26. Izotermická expanze – vratná
Izotermická komprese
+
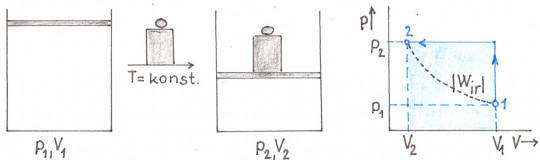
Obr. 27. Izotermická komprese – nevratná
+
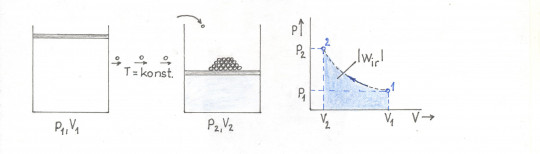
Obr. 28. Izotermická komprese – vratná
Příklad
Příklad 5.3
2,5 molu ideálního plynu se při teplotě 20 °C izotermicky rozpíná z objemu 30 litrů na objem 58 litrů. Jakou práci soustava vykoná při nevratném a vratném průběhu děje?
Zobrazit řešení
Skrýt řešení
Řešení
ze zadání:
n = 2,5 mol
t =20 °C; T = 273 + 20 = 293 K
V1 = 30 l = 0,03 m3 =30∙10-3 m3
V2 = 58 l = 0,058 m3
Wire = ?
Wrev = ?
výpočet:
- nevratná/ireverzibilní expanze
p2 = ?
ze stavové rovnice:
- vratná/reverzibilní expanze
Soustava vykoná při nevratné expanzi práci 2,94 kJ a při vratné 4,01 kJ.
Příklad
Příklad 5.4
5 molů ideálního plynu za izotermních podmínek při teplotě 300 K změnilo svůj objem. Původní tlak plynu byl 0,08 MPa a konečný tlak 170,4 kPa. Došlo k expanzi nebo ke kompresi plynu? Vypočítej práci konanou/dodanou při nevratném ději a při vratném ději.
Zobrazit řešení
Skrýt řešení
Řešení
ze zadání:
n = 5 mol
T = 300 K
p1 = 0,08 MPa = 0,08 ∙ 106 Pa = 80 000 = 80 kPa
p2 = 170,4 kPa = 170,4 ∙ 103 Pa = 170 400 Pa
výpočet:
p2 > p1 => jedná se o kompresi plynu
- nevratná:
Práce vyšla kladně – jedná se o dodanou práci plynu.
Práce dodaná při nevratné kompresi je 14,09 kJ.
- vratná:
Práce dodaná při vratné kompresi je 9,43 kJ. Ve srovnání s nevratnou kompresí je menší.
5.2.4.2
Izochorický děj, V = konst.
Jestliže se nemění objem (ΔV = 0), tak plyn nekoná práci. W = 0. Po dosazení do 1. termodynamické věty, dostáváme:
Definice
Teplo Q vyměňované mezi soustavou a okolím při izochorickém ději se rovná změně vnitřní energie ΔU.
Znamená to, že teplo dodané soustavě za konstantního objemu se využije k jejímu ohřevu.
5.2.4.3
Izobarický děj, p = konst.
Do vztahu pro 1. termodynamickou větu ΔU = Q + W dosadíme za práci W vztah pro objemovou práci – p ∙ ΔV. Dále pokračujeme odvozováním:
H ... entalpie, extenzivní stavová funkce; lze měřit pouze změnu entalpie.
5.2.4.4
Entalpie
Definice
Teplo Q vyměněné mezi soustavou a okolím při izobarickém ději se rovná změně entalpie ΔH. Jednotkou entalpie je joule (J) [džaul].
Může nastat:
ΔH > 0, pak soustava při chemické reakci teplo přijímá ... endotermická (endotermní) reakce
ΔH < 0, pak soustava při chemické reakci teplo odevzdává, uvolňuje ... exotermická (exotermní) reakce
5.2.4.5
Adiabatický děj
Adiabatický děj probíhá v tepelně izolovaných soustavách. Při adiabatickém ději nedochází k výměně tepla mezi systémem a okolím.
Po dosazení do 1. termodynamické věty:
Adiabaticky přijatou prací (při adiabatické kompresi) soustava zvyšuje svou vnitřní energii a ohřívá se. Pokud koná soustava adiabatickou práci (při expanzi), koná ji na úkor své vnitřní energie, takže se ochlazuje.
V případě ideálního plynu platí:
Cv ...izochorická molární tepelná kapacita
Adiabaticky izolovaný ideální plyn se při expanzi ochlazuje (ΔT < 0) a koná práci (W< 0) na úkor své vnitřní energie (ΔU < 0, Cv > 0). Při adiabatické kompresi je tomu opačně.
Probíhá-li adiabatická expanze nebo komprese ideálního plynu reverzibilně, platí pro jeho tlak a objem Poissonovy rovnice.
κ ... [čti kapa] se nazývá Poissonova konstanta
Cp ...izobarická molární tepelná kapacita
cp ...izobarická měrná tepelná kapacita
cv ...izochorická měrná tepelná kapacita
Pro jednoatomové ideální plyny je hodnota
, pro dvouatomové molekuly
.
Pamatujte si, že Poissonovy rovnice platí pokud:
- se jedná o adiabatický vratný děj,
- počítáme s ideálním plynem,
- tepelné kapacity nezávisí na teplotě,
- se koná jen objemová práce.
Není-li jediná z podmínek splněna, Poissonovy rovnice neplatí.
5.2.5
Teplo
V kapitole 5.2 prvního termodynamického zákona se mluví o teplu. Teplo je možné kalorimetricky změřit. Pro výpočty je třeba znát také tepelnou kapacitu látek.
5.2.5.1
Tepelná kapacita
Každá látka potřebuje k ohřátí o určitou teplotu jiné množství tepla. Proto byla zavedena tepelná kapacita. Značíme ji K.
Definice
Tepelná kapacita je fyzikální veličina vyjadřující množství tepla potřebného k ohřátí soustavy o 1 K (Kelvin), respektive o 1 °C, neboť ΔT = Δt.
Q ... teplo, které soustava přijala při ohřátí o
teplotní interval vyjadřující, o kolik se zvýšila teplota:
Tepelná kapacita má jednotku J ∙ K-1. V uvedeném matematickém tvaru odpovídá celé soustavě. V praxi se používají tabelované hodnoty, které jsou vztažené na jednotku hmotnosti nebo na 1 mol.
Definice
Specifická (měrná) tepelná kapacita c udává množství tepla potřebného k ohřátí 1 kg látky o 1 K.
Definice
Molární tepelná kapacita C udává množství tepla potřebného k ohřátí 1 molu látky o 1K.
Poznámka
Hodnoty tepelných kapacit v tabulkách bývají označeny indexy p nebo V. Znamenají, že hodnoty byly stanoveny při konstantním tlaku nebo objemu.
Tabulka 5. Tepelné kapacity vybraných látek
látka | c [J ∙ K-1 ∙ kg-1] |
voda | 4180 |
led | 2090 |
měď | 383 |
olovo | 129 |
ethanol | 2430 |
beton | 800-1100 |
Zkusme se zamyslet nad hodnotami v tabulce:
- Vyšší hodnoty c značí podle definice potřebu dodání většího množství tepla k ohřátí o 1 °C nebo 1 K.
- Led má poloviční tepelnou kapacitu v porovnání s vodou. Proto je k ohřátí vody o 1°C potřeba dvojnásobné množství tepla oproti ohřátí ledu o 1 °C. (Může jít o libovolný 1°C, např. ohřev ledu z -10 °C na -9 °C a vody z 62 °C na 63 °C. Zde samozřejmě uvažujeme jen o teplotách, kdy je led ledem a voda vodou, neuvažujeme o skupenských přeměnách.)
- Beton má 4x – 5x menší hodnotu než voda, a tak se nelze divit, že v létě není až tak nesnadné jej v ulicích rozehřát.
- Voda má poměrně velkou tepelnou kapacitu, proto je energeticky náročné ji ohřát. Využívá se jako chladicí médium (odebere hodně tepla a moc se neohřeje) – viz např. při destilaci, k chlazení motorů, jaderných reaktorů aj.
- Také pranostika „Únor bílý, pole sílí“ souvisí s tepelnou kapacitou. Sníh na poli působí jako izolant a brání vymrznutí půdy. Teplota pod sněhem je okolo 0 °C. Pokud by vrstva sněhu na poli neležela, v půdě by klesla teplota podle okolní třeba až na –20 °C. Mluvili bychom o tzv. holomrazech.
- Sníh a led jako izolant využívají i Eskymáci. Za polární zimy klesá teplota venku až na – 60 °C. Na vnitřní straně iglú má led 0 °C. Vyšší teplotu led mít nemůže, protože by začal tát. Eskymáci vykládají stěny kožešinami. Když zapálí několik lampiček na tulení tuk, teplota uvnitř iglú je pak i přes 20 °C.
- Teplé oblečení nošené v zimě také využíváme jako izolant. Ztrácíme méně tepla, „cítíme se zahříváni“.
- U látek s vysokou hodnotou tepelné kapacity trvá déle, než se ohřejí, ale pak také pozvolna chladnou. Což lze pozorovat v přímořských oblastech, kde jsou v porovnání s vnitrozemním podnebím menší rozdíly mezi denní a noční teplotou nebo letními a zimními teplotami.
5.2.5.2
Kalorimetrie a kalorimetrická rovnice
Kalorimetrie je část termiky, která se zabývá měřením tepla. K měření se používá kalorimetr, což je v podstatě tepelně izolovaná nádoba. V laboratorním a průmyslovém prostředí se pro tepelně izolovanou nádobu používá název Dewarova nádoba neboli „dewarka“. Mohou mít kovový plášť a uvnitř super izolační fólií ve vakuovaném prostoru, nebo skleněnou nádobu s dvojitými postříbřenými stěnami a vakuovaným prostorem mezi nimi, takže odrážejí vnější i vnitřní tepelné vyzařování. Z domácnosti ji známe v podobě termosky.
Měření tepla se skládá ze dvou částí:
- Stanovení tepelné kapacity kalorimetru K pomocí teplé a studené vody:
Příklad
Zobrazit řešení
Skrýt řešení
Řešení
m1... hmotnost studené vody na začátku měření (t ≅ 16 °C)
m2 ... hmotnost teplé vody přidávané k soustavě (t ≅ 28 °C)
K ... tepelná kapacita kalorimetru
c ... specifická tepelná kapacita vody
t1 ... naměřená teplota na začátku měření
t2 ... naměřená teplota přidávané vody
t ... naměřená teplota po ustálení nebo zjištěná graficky z naměřených hodnot
- Vlastní měření tepla ΔH (neutralizačního, rozpouštěcího, spalného, ...):
Příklad
Výsledek v J přepočteme na J ∙ g-1 nebo J ∙ mol-1.
Zobrazit řešení
Skrýt řešení
Řešení
Δt ... rozdíl teplot na začátku měření a po ustálení, popř. z grafu
m ... hmotnost reakční směsi
+
![29. Části kalorimetru [30]](image/small/img029.png)
Obr. 29. Části kalorimetru [30]