3.3
Detekce patogenních mikroorganismů v potravinách
Souhrn
Mikroorganismy můžeme stanovit různými způsoby. Záleží hlavně na účelu, jemuž budou získané výsledky sloužit. Podle vybavení každé laboratoře je možné metody různě kombinovat, aby bylo dosaženo co nejpřesnějších výsledků. Metody můžeme rozdělit do několika skupin.
Metody přímé nebo také mikroskopické jsou založeny na zjišťování jednotlivých buněk nebo mikrokolonií mikroskopem. Mohou být kvantitativní (zjištění počtu) i kvalitativní (rozlišení tvaru, velikosti, uspořádání i barvitelnosti buněk).
Metody nepřímé jsou založeny na některých projevech biochemické aktivity, na tvorbě kolonií apod. Můžeme jimi stanovit jak počet mikroorganismů, tak i druhové nebo skupinové zastoupení. Tyto metody se mohou rozdělovat na přesné, kultivační a technické i orientační. Kultivační metody mohou být plotnové nebo zkumavkové. Technické metody mohou být papírkové, enzymové a termostatové. Používají se i automatizované metody a různé mikrometody.
Vedle klasických metod, které k průkazu patogenních mikroorganismů v potravinách potřebují 5 – 10 dní se používají i rychlé metody. Výhodou rychlých metod je rychlé získání negativních výsledků, tj. zjištění nepřítomnosti příslušného patogenního mikroorganismu v potravině. Pozitivní výsledek vyžaduje další vyšetření vzorku obvykle opět klasickou metodou.
3.3.1
Rychlé metody
3.3.1.1
Chromogenní a fluorogenní živné půdy
Chromogenní média slouží k rychlé a jednoduché detekci bakterií pomocí chromogenních substrátů v půdě. Živné půdy obsahují substrát MUG (4-methyl-umbelliferyl-β-D-glukuronid) a ten je štěpen enzymem glukuronidasa za vzniku metabolitu. Chromogenní živná půda vytváří specifické zabarvení.
Příklad
Např. Chromocult firmy Merck obsahuje Salmon-Gal, který koliformní bakterie štěpí za vzniku červené barvy a obsahuje MUG, který enzym β-D-glukuronidasa štěpí za vzniku modré barvy. Vzhled kolonií a hodnocení po kultivaci je tedy následující.
Červené kolonie - koliformní bakterie (mají enzym β-D-galaktosidasa, štěpí Salmon-Gal)
Sytě fialově modré - Escherichia coli (má oba enzymy, kombinace modré a červené barvy)
Světle modré - r. Salmonella (má enzym β-D-glukuronidasa, ale nemá enzym β-D-galaktosidasa)
Bezbarvé kolonie - ostatní zástupci č. Enterobacteriaceae, nemají žádný z enzymů
+
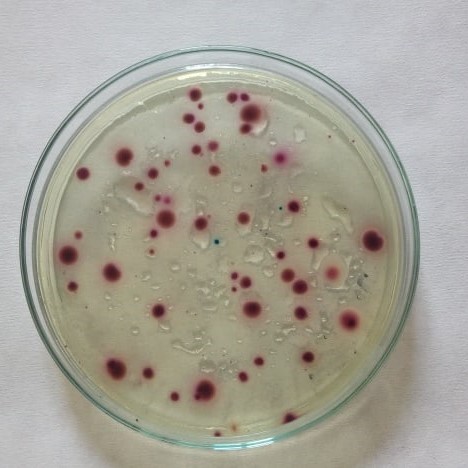
Obr. 16. Koliformní bakterie na živné půdě Chromocult
+
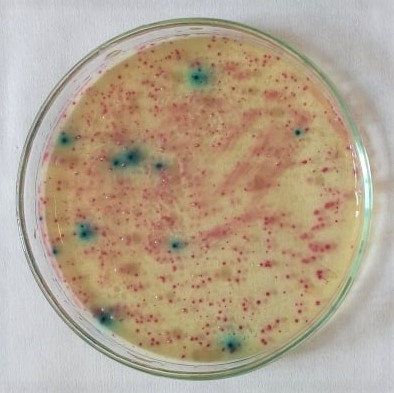
Obr. 17. Escherichia coli na živné půdě Chromocult
Fluorogenní živné půdy se skládají ze specifického substrátu pro určitý enzym jako je cukr nebo aminokyselina a fluorescenčního barviva (4-methylumbelliferon), které je schopno přeměnit UV (ultrafialové) záření ve viditelné světlo. Fluorogenní živná půda fluoreskuje po ozáření UV světlem (360 nm).
3.3.1.2
Hygicult
Hygicult je plastová destička po obou stranách pokrytá živnou půdou a umístěná v plastové sterilní zkumavce uzavřené šroubovacím uzávěrem. Používá se k rychlému monitorování úrovně mikrobiální kontaminace v potravinářských provozech a monitorování hygienické nezávadnosti kapalin. Výhodou je snadné použití mimo laboratoř. Jedna zkumavka umožňuje odběr a kultivaci dvou vzorků. Vzorek můžeme odebrat třemi různými způsoby. Buď pomocí stěru, ponořením do kapaliny, nebo přímo otiskem pevného povrchu. Vyhodnocení výsledků se provádí pomocí vzorové tabulky. Není tedy nutné počítat kolonie.
3.3.1.3
Petrifilm
Petrifilmy jsou destičky pro přesnou kontrolu mikrobiologické kvality potravin nebo prostředí potravinářských provozů. Destičky se skládají ze dvou vrstev filmů, které obsahují živné půdy, gel rozpustný ve studené vodě a speciální indikátor, který zvýrazní narostlé kolonie mikroorganismů na destičce. Natištěná mřížka usnadní počítání kolonií. Stanovujeme pomocí nich počty různých druhů a skupin mikroorganismů a zjišťujeme mikrobiální kontaminaci prostředí. Vzorek se naředí a homogenizuje. Pak se sterilní pipetou napipetuje 1 ml takto upraveného vzorku do středu kultivační destičky. Opatrně přiklopíme vrchním filmem tak, abychom zabránili tvorbě vzduchových bublin. Plastovým roztlačovačem následně vzorek rozprostřeme po celé ploše kruhové destičky. Kultivujeme vrchní stranou nahoru ve sloupcích po maximálně 20 kusech. Po kultivaci spočítáme charakteristické kolonie, které mohou být podrobeny další identifikaci. Když testujeme hygienu prostředí, nejprve navlhčíme destičku přidáním 1 ml fyziologického roztoku, který roztlačíme po celém povrchu destičky. Takto připravený nosič lze použít jak pro metodu stěrovou a otiskovou tak pro hodnocení spadu z ovzduší.
Příklad
Pomocí Petrifilmu určujeme celkový počet mikroorganismů, počet bakterií čeledi Enterobacteriaceae, koliformních bakterií a Escherichia coli, počet Staphylococcus aureus, Listeria spp. či počet kvasinek a plísní.
+

Obr. 18. Petrifilm
+

Obr. 19. Koliformní bakterie na Petrifilmu
3.3.1.4
Polymerázová řetězová reakce
Principem PCR (polymerázová řetězová reakce) je replikace (zdvojení) molekuly DNA (deoxyribonukleová kyselina), která pravidelně nastává v živých buňkách před jejich rozdělením na dvě nové (dceřiné) buňky. Při PCR je tato replikace uměle navozena ve zkumavce (in vitro) a její průběh je kontrolován změnami teplot. Předpokladem pro to je zajištění optimálního prostředí pro reakci, včetně velmi přesné kontroly teploty v jejím průběhu, dodání potřebných stavebních kamenů pro vytvoření kopírované DNA a zejména dodání malých kousků DNA, tzv. primerů, které jsou schopny takovou reakci zahájit [11].
Souhrn
Každý mikroorganismus má charakteristický úsek DNA (gen), pomocí kterého se identifikuje. Tento úsek DNA se polymeruje (pomnoží) a detekuje. Tak se určí neznámý mikroorganismus. Tedy z genetické výbavy buňky se získá jeden charakteristický úsek DNA a ten se namnoží a stanoví (detekuje).
Příklad
Metoda se používá k identifikaci patogenních mikroorganismů a virů jako například salmonely, legionely, listerie, Escherichia coli, Staphylococcus aureus, Campylobacter, mykobakterie, HIV, rickettsie aj. Vyhledávají se v potravinářském nebo klinickém materiálu, pomáhá při odhalování falšování potravin, přítomnost GMO (geneticky modifikované organismy)apod.
Postup:
Nejdříve se musí upravit vzorek a to tak, že se usmrtí všechny přítomné mikroorganismy a provede se lyzování buněk a extrakce DNA. Celý proces probíhá ve zkumavce, takže není žádné hygienické riziko. Mikrobiální DNA se denaturuje zahřátím, dvoušroubovice se oddělí a pomocí DNA polymerázy se nasyntetizuje protilehlý řetězec ze základních stavebních prvků:
Příklad
z 1 DNA denaturace → 2 DNA denaturace → 4 DNA → 8 DNA → 16 DNA po 20 denaturacích → 106 DNA
Krátké řetězce nukleotidů tzv. primery se naváží na denaturovanou DNA na začátek a konec hledaného úseku DNA a vymezí činnost DNA polymerázy na vybraném úseku.
Proběhne amplifikace, což je kopírování nebo klonování charakteristických sekvencí DNA.
Zajímavost
DNA polymeráza je enzym získaný z bakterie Thermus aquaticus, který se nachází v horkých pramenech, v sopečnatých oblastech oceánů. Získaný enzym je termostabilní a uchovává si svou aktivitu i přes působení vysokých teplot během probíhajících reakcí.
K detekci dochází pomocí metod k určení přítomnosti sekvence DNA jako například gelová elektroforéza, genosondy a fluorescenční barviva. Výsledek stanovení je znám asi za 3 – 24 hodin.
3.3.1.5
Bioluminiscenční metody
Souhrn
Principem je, že počet mikroorganismů se měří podle množství ATP (adenosintrifosfát) ve vzorku. Hladina ATP je ve všech buňkách relativně stejná, proto množství ATP lze posuzovat jako množství buněk ve vzorku. ATP je zkratka pro adenosintrifosfát tedy adenin, ribóza a tři zbytky kyseliny fosforečné vázané kovalentní chemickou vazbou. Adenosintrifosfát přenáší energii z exergonických reakcí do endergonických (katabolismus – anabolismus).
Luminiscence je schopnost některých látek po dodání energie vyzařovat elektromagnetické záření tedy světlo a spontánně světélkovat. Tento jev je běžný u živých organismů jako například medúzy, světlušky nebo některé hlubokomořské ryby.
Luciferiny jsou látky, které mají schopnost přecházet do excitovaného stavu tedy záření a energie se uvolňuje jako viditelné záření.
Luciferázy jsou enzymy, které katalyzují přeměnu luciferinu do excitovaného stavu a energie se z ATP přemění na světelnou.
Takže při setkání vzorku s adenosintrifosfátem a luciferinem a luciferázou vznikne světlo tedy luminiscence.
Příklad
U těchto metod se používají tzv. luminometry, což jsou přístroje, které měří intenzitu bioluminiscence a světelná kvanta uvolněná excitovaným luciferinem se měří v relativních světelných jednotkách (RLU). Kalibrace přístroje odpovídá počtu mikroorganismů nebo buněk.
Bioluminiscenčními metodami se stanovuje například mikrobiální nebo nemikrobiální kontaminace, sleduje se celková kontaminace ploch i strojů nebo zařízení. Dále pak se kontroluje účinnost čistících postupů, stanovuje se celkový počet mikroorganismů nebo počet somatických buněk ve mléce.
3.3.1.6
Imunochemické metody
Souhrn
Imunochemické metody se používají ke zjišťování sérotypu jednotlivých patogenních bakterií z potravin nebo klinického materiálu. Imunochemické postupy slouží pro detekci nebo zjišťování počtu, druhu, rodu mikroorganismů a jejich toxinů.
Antigen je látka, která vyvolává imunitní reakci s tvorbou protilátek.
Imunogen je látka schopná vyvolat v organismu obrannou reakci imunitního systému, jejíž součástí je produkce protilátek lymfocyty.
Zajímavost
Imunogen má vždy vlastnosti antigenu, zatímco ne všechny antigeny vyvolávají tvorbu protilátek.
Protilátka (imunoglobulin) je bílkovina krevního séra (glykoprotein), která specificky váže antigen, na jehož podnět byly organismem vytvořeny.
Metody používané k detekci:
- RIA – radioimunologická
- FIA – fluorescenční
ELISA má široké uplatnění v diagnostice bakteriálních, virových i parazitálních onemocnění. Uplatňuje se rovněž při průkazu neinfekčních antigenů (pohlavních hormonů, inzulinu, fotoproteinu, aj.) i v diagnostice alergických a autoimunitních chorob.
Příklad
V potravinářské mikrobiologii se používá ke zjištění například salmonel, listerií, kampilobakterů, botulotoxinů, shigelotoxinů a dalších.
Podstatou je, že antigen vyvolá tvorbu protilátek u mikroorganismu specifickým procesem. Při této reakci je jedna ze složek fixovaná na nosič tedy na dno zkumavky nebo mikrotitrační destičky. Na pevnou fázi, která je nasycena specifickou protilátkou se naváže buď standardní, nebo stanovovaný antigen. Po inkubaci a promytí se na navázaný antigen fixuje specifická protilátka proti příslušnému antigenu, značená enzymem (konjugát). Nejčastěji se používá enzym peroxidáza nebo alkalická fosfatáza. Po další inkubaci a následném promytí, kterým je odstraněn nenavázaný konjugát se přidá substrát a indikátor, který po účinku enzymů na substrát změní barvu. Barevné změny se hodnotí pouhým okem nebo přesněji fotometricky. Intenzita barevné změny je přímo úměrná množství vázaných molekul konjugátu na komplexní antigen-protilátka a tedy i množství antigenu ve vzorku.
Nejčastěji se používá standardní sendvičová ELISA na zjištění koncentrace antigenu. Nejdříve dojde k navázání protilátky na dno zkumavky. Pak se přidá vzorek a inkubuje. Tím dojde ke vzniku vazby antigen-protilátka. Provede se odmytí nenavázaného antigenu a přidá se druhá protilátka, která váže stejný antigen, na které je kovalentně připojen enzym. Opět se inkubuje a odmyje nadbytečná protilátka s enzymem. Přidá se substrát a proběhne enzymem katalyzovaná reakce. Na závěr dojde k zastavení reakce a měření. Jako sendvičová se nazývá proto, že antigen je jako sendvič mezi dvěma protilátkami. Obdobně lze reakci provést na detekci protilátek ve vzorku. To probíhá obdobně, jen je v 1. kroku navázán na zkumavku antigen a druhá protilátka je proti hledané protilátce. Tato metoda se označuje jako capture ELISA [11].
RIA metoda se využívá při stanovení aflatoxinů produkovaných plísněmi Aspergillus flavus. A antigen je zde označen radionuklidem. Princip metody je podobný jako u metody ELISA, ale protilátka je značena radioaktivními izotopy. Reakce je velmi citlivá a přesná, výsledek je vyhodnocován počítačem tedy počtem impulsů γ (gama) záření. Pracoviště musí být speciálně vybaveno pro práci s radioaktivními izotopy. Nyní je většina těchto metod nahrazena metodami enzymové imunoanalýzy.
3.3.1.7
Fluorescenční metody
Nejznámější fluorescenční imunologická metoda je ELFA (Enzyme-Linked Fluorescent Assay). Princip této metody je podobný jako u metody ELISA, rozdíl je jen v použitém substrátu, který je enzymem štěpen na fluorescenční produkt. Vzniklé chemické změny jsou detegovány pomocí fotodiodového fluorimetru. ELFA využívá například systém VIDAS (VITEK, Francie), který má široké využití v klinické mikrobiologii. Pro potravinářskou mikrobiologii jsou vyvinuty VIDAS kity pro stanovení salmonel, kampylobakterů, Listeria spp., Listeria monocytogenes, Escherichia coli O157 a stafylokokových enterotoxinů. Technika VIDAS se skládá ze dvou částí. Používá sendvičovou techniku k zachycení antigenu nebo toxinu patogenních mikroorganismů mezi potaženými protilátkami a protilátkami konjugovanými s enzymem, který slouží jako indikátor. A ve druhé části se měří intenzita fluorescence plynoucí z katalýzy substrátu konjugovanými enzymy [12].
3.3.1.8
Průtoková cytometrie
Metoda založená na analytické a preparativní technice umožňující rychlá měření optických vlastností buněk. Moderní cytometry jsou podmíněny pokroky v oblasti optiky, elektroniky a fluidity. Kromě rychlosti analýz, která může dosahovat několik desítek tisíc částic za sekundu je předností i schopnost třídit mikroskopické částice podle jejich vlastností v reálném čase. Parametrem průtokové cytometrie může být například granularita, obsah DNA, životnost a pH buněk a to vše se může označit protilátkou.
Průtoková cytometrie, je založena na zachycení rozptylu světla bakteriálními buňkami s navázanými protilátkami značenými fluorescenčními barvivy. K dispozici jsou značené protilátky proti patogenům salmonel, listerií a kampylobakterů.
3.3.1.9
Impedanční metody
Jsou založené na změně vodivosti prostředí činností mikroorganismů. V živném prostředí se v důsledku enzymové činnosti bakterií mění elektricky inertní (nevodivé) molekuly substrátu v ionizované (vodivé) sloučeniny (např. cukry v organické kyseliny). Tím se zmenšuje odpor, který klade prostředí průchodu elektrického proudu. Změny lze stanovit pomocí elektrod. Měřící, přístroje umožňují automaticky proměřovat impedanci (celkový odpor prostředí). Sleduje se čas potřebný k tomu, aby počáteční inokulum dosáhlo prahové hodnoty (detekční čas impedance) a impedanční profil – průběh změn impedance v závislosti na čase během růstu kultury a celkový rozsah změny vodivosti. Čím vyšší je počet mikroorganismů, tím je doba detekce kratší. Podle kalibrační křivky pro různý počet mikroorganismů se automaticky stanoví počet mikroorganismů ve vzorku. Využívá se ke zjištění přítomnosti salmonel, listerií a koliformních bakterií.
3.3.1.10
Imunomagnetická separace
IMS (imunomagnetická separace) je metoda založená na principu vazby bakteriálních buněk na magnetické částice s imobilizovanými specifickými protilátkami. Vzniklý komplex je možné separovat ze suspenze pomocí vnějšího magnetického pole. Tato specifická separační technika umožňuje významné selektivní zkoncentrování cílových buněk. Díky tomu lze imunomagnetické separace úspěšně využít jako náhradu kroku selektivního pomnožení při kultivačním vyšetření významných patogenů [13].
3.3.1.11
Reverzní pasivní latexová aglutinace
Souhrn
RPLA (reverzní pasivní latexová aglutinace) je založena na reakci antigenu v roztoku (toxinu) s protilátkami, které jsou navázány na latexové částice. Metoda se provádí v mikrotitračních destičkách, jejichž jamky mají kónické dno. Je-li toxin ve vzorku obsažen, protilátka aglutinuje a klesá na dno reakční jamky, kde utváří charakteristickou sraženinu.
Podle typu aglutinace rozlišujeme O-aglutinaci, při které se bakterie váží celými těly (somatický antigen O), nebo H-aglutinaci, kdy se bakterie váží svými bičíky (flagelární antigen H). V některých případech může docházet k aglutinaci bakteriální suspenze ve fyziologickém roztoku i bez přítomnosti protilátek, tento jev nazýváme autoaglutinace. Naopak anaglutinabilita je jev, při kterém kapsulární antigen pokrývá povrch somatického antigenu a bakteriální kmen s přidanou protilátkou neaglutinuje. Aglutinační reakce lze obecně využít pro sérologickou identifikaci a typizaci bakterií (např. salmonel, kampylobakterů, Escherichia coli) nebo naopak k průkazu přítomnosti specifických protilátek v krevním séru. Metoda RPLA se používá nejen k průkazu patogenních mikroorganismů, ale i jejich toxinů v potravinách [14].
3.3.1.12
Imunochromatografické metody
U imunochromatografických metod reaguje antigen přítomný ve sledovaném vzorku s konjugátem za vzniku komplexu antigen-konjugát, který migruje směrem k specifickému proteinu imobilizovanému na porézní membráně (nitrocelulóza). Je-li ve vzorku přítomen antigen, vznikne v místě navázání komplexu antigen-konjugát na imobilizovaný protein specifický band, signalizující pozitivní výsledek. Nadbytek konjugátu přítomného v testu, migruje dále membránou a váže se na jiný imobilizovaný protein za vzniku druhého bandu, který signalizuje ukončení testu [15]. Nejčastěji se tato metoda používá pro detekci patogenních mikroorganismů v potravinách, např. salmonel, listerií, Escherichia coli O157 či kampylobakterů. Dále lze tuto metodu použít i pro stanovení bakteriálních toxinů, např. verotoxinů VT1 a VT2.