1.3
Faktory ovlivňující přežívání mikroorganismů v potravinách
Přežívání mikroorganismů v potravinách závisí na vnitřních a vnějších faktorech. Určují nám druh změn, rychlost růstu a množení mikroorganismů. Působení mikroorganismů nám může měnit vlastnosti potraviny a způsobit jejich kažení. Technologické postupy výroby jsou sestavené tak, aby se zamezilo přežívání mikroorganismů v potravinách a jejich následnému růstu.
- Vnitřní faktory se nejvíce projevují při zpracování potravin. Mezi vnitřní faktory patří složení potraviny, aktivita vody, aktivní kyselost, redoxní potenciál, textura a obsah přirozených antimikrobních látek.
- Vnější faktory působí hlavně při skladování a uchovávání potravin. Patří mezi ně teplota, relativní vlhkost, složení atmosféry v obalu a skladovacím prostoru a čas [2, 5].
Dalšími faktory, které ovlivňují přežívání mikroorganismů v potravinách, jsou mechanické vlivy, tlak, záření, působení cizorodých antimikrobních látek, dezinfekční prostředky a další.
1.3.1
Technologicky významné změny v potravinách
Změny, ke kterým dochází v potravinách, jsou:
- fyziologické,
- enzymové,
- chemické,
- mikrobiologické.
1.3.1.1
Fyziologické změny
Jsou pochody, které navazují na fyziologické procesy v živých rostlinných pletivech a živočišných tkáních při narušení podmínek zpracování a skladování [6].
Příklad
Uplatňují se u čerstvého ovoce, zeleniny a u masa po porážce [6].
1.3.1.2
Enzymové změny
Jedná se o dílčí reakce způsobené přirozenými enzymy, případně extracelulárními enzymy produkovanými přítomnou mikroflórou. Obvykle se enzymové změny uplatní po mechanickém porušení pletiva v důsledku technologických operací (loupání, dělení, lisování, ale také pomalé zmrazování – vlivem tvorby velkých krystalů ledu). Enzymové procesy jsou přerušeny inaktivací enzymů, nejčastěji záhřevem [6].
Příklad
Při skladování potravin se uplatňují zejména u čerstvého ovoce a zeleniny a u výrobků, u kterých nedošlo k dostatečné inaktivaci před dalším zpracováním (zmrazováním, sušením apod.) [6].
1.3.1.3
Chemické změny
Na změnách potravin během zpracování a skladování se podílí také vzájemné chemické reakce všech složek potraviny, kterých se účastní také produkty fyziologických a enzymových procesů, látky přicházejí do potraviny zvenčí (kyslík, složky obalů, kontaminující látky apod.) a také produkty metabolismu přítomných mikroorganismů [6].
Poznámka
Chemické změny jsou často faktorem, který limituje skladovatelnost potravinářských produktů [6].
1.3.1.4
Mikrobiologické změny
Mikrobiologické změny jsou prakticky nejvýznamnější změny s ohledem na ovlivnění jakosti a zdravotní nezávadnosti. Dochází při nich ke snížení nutriční a senzorické hodnoty potraviny. Potravinářské suroviny, polotovary a výrobky obsahují mikroorganismy nebo jejich zárodky. Součástí každého technologického zpracování je vždy konzervační zákrok, který zastaví nebo zpomalí nežádoucí růst mikroorganismů, případně usmrtí ty formy, které by se za podmínek skladování mohly množit a potravinu kazit [6].
1.3.2
Vnější faktory
1.3.2.1
Teplota
Je jeden z nejdůležitějších faktorů vnějšího prostředí, který ovlivňuje rychlost rozmnožování a život mikroorganismu. Teploty, které umožňují růst mikroorganismů, se pohybují od 0 °C do 90 °C, i když byly popsány ještě vyšší teploty, při kterých některé druhy bakterií rostou a žijí. Hodnotíme-li závislost růstu na teplotě, určují se tři základní teploty:
- minimální, tj. nejnižší teplota, při které se mikroorganismus ještě rozmnožuje měřitelnou rychlostí;
- optimální, tj. teplota, při níž se mikroorganismus rozmnožuje největší rychlostí;
- maximální, tj. nejvyšší teplota, při které je mikroorganismus ještě schopen se rozmnožovat.
Optimální teploty pro jednotlivé fyziologické pochody v buňce se liší pro každý druh. Účinek teploty je rovněž ovlivněn velikostí kultivační nádoby, koncentrací buněk, obsahem vody v živném substrátu a pH. Obvykle se stanovuje optimální teplota růstu, smrtící teplota a méně často teplotní rozmezí růstu.
Poznámka
Optimální teplota pro rozmnožování se nemusí vždy shodovat s optimální teplotou pro ostatní životní procesy buňky [1].
Definice
Smrtící (letální) teplota je nejnižší teplota, která během určité doby usmrcuje mikroorganismus za přesně definovaných podmínek.
Smrtící teplota se pro jednotlivé mikroorganismy liší a je ovlivněna koncentrací buněk, fyziologickým stavem kultury (stářím), složením média a pH. Obvykle se smrtící teplotou rozumí teplota, která za 10 minut usmrtí všechny buňky v suspenzi. Z technologického hlediska má větší význam stanovení nejkratší doby, která je potřebná k usmrcení mikroorganismů za dané teploty a definovaných podmínek, tzv. smrtící doby. Velká většina mikroorganismů patří mezi mezofilní, které jsou usmrcovány teplotami kolem 60 °C působícími 10 až 15 minut. Odolnost mikroorganismů k teplotě ovlivňuje obsah vody v prostředí i v buňkách, pH prostředí a přítomnost některých látek (lipidy, bílkoviny, sacharidy) ve vyšší koncentraci.
Rozdělení mikroorganismů podle vztahu k teplotě:
- Psychrofilní mikroorganismy
- Psychrotrofní mikroorganismy
- Mezofilní mikroorganismy
- Termofilní mikroorganismy
- Hypertermofilní mikroorganismy
+
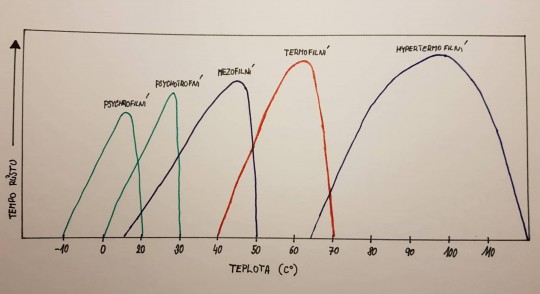
Obr. 2. Rozdělení mikroorganismů podle vztahu k teplotě
Poznámka
Mezi průměrnou minimální a průměrnou optimální teplotou je průměrný rozdíl 22 °C a mezi průměrnou optimální a maximální teplotou je průměrný rozdíl 6,5 °C.
Významné postavení v mikrobiologii potravin má skupina psychrotrofních bakterií. Jsou schopné růstu při teplotách mezi 0–5 °C, přestože se mohou množit až do teplot 43 °C a jedná se tedy de facto o mezofilní mikroorganismy. Na rozdíl od psychrofilních mikroorganismů, které se nachází v potravinách pocházejících z extrémně chladného prostředí, příčinou kažení masa, zeleniny a dalších potravin skladovaných při teplotách 0–5 °C jsou zpravidla psychrotrofy [1].
Příklad
Gramnegativní tyčinky z rodu Pseudomonas, Acinetobacter, Moraxella, Aeromonas, Vibrio, Serratia, apod. vykazují nejčastěji psychrotrofní růst. Také některé kmeny rodu Bacillus a Lactobacillus, některé enterokoky a mikrokoky. Extrémně psychrotrofní jsou kvasinky, některé mohou růst i při –10 °C, podobně i některé plísně. Mezi patogenní psychrotrofy patří Clostridium botulinum typ E, Yersinia enterocolitica a Listeria monocytogenes. Závěrem je třeba říci, že většina bakterií způsobujících onemocnění z potravin patří do skupiny mezofilních mikroorganismů a při dodržení chladicího řetězce se nemnoží [2].
Tabulka 1. Působení teplot na růst mikroorganismů
Teplota °C | Projev |
–18 až 0 | Zastavení růstu mikroorganismů, částečné fungování látkové výměny. Metabolismus zpravidla zastaven při –18 °C. |
–5 až 0 | Velmi pomalý růst vybraných mikroorganismů. |
0 až 15 | Pomalý růst omezeného spektra mikroorganismů. |
15 až 50 | Optimální podmínky pro růst mikroorganismů. |
50 až 65 | Minimální růst omezeného spektra mikroorganismů. |
65 až 80 | Zastavení růstu většiny mikroorganismů. |
65 až 100 | Podle podmínek (doby záhřevu) usmrcena většina vegetativních buněk a spor některých bakterií. |
Více než 100 | Usmrceny buňky mikroorganismů a podle podmínek také spory bakterií. |
Působení nízkých teplot
Nižší než optimální teploty přežívá většina mikroorganismů poměrně dlouhou dobu. Přenesou-li se však z optimálních teplot do teploty kolem 0 °C dochází k chladovému šoku [1].
Zajímavost
Významnou částí buněčné populace na Zemi jsou psychrofilní mikroorganismy. Více než 80 % zemského povrchu je vystaveno trvalému působení teplot nepřesahujících průměrnou teplotu 5 °C.
Příklad
Při pomalém zmrazování mikroorganismů na teploty pod 0 °C se z vnitrobuněčné i mimobuněčné vody tvoří velké krystaly ledu, které buňku nevratně poškozují. Rychlé zmrazování buněk na teploty –30 °C až –180 °C způsobuje tvorbu mikrokrystalků ledu a ty buňky mikroorganismů poškozují jen minimálně. Rychlé zmrazení buněk mikroorganismů v roztoku peptonu nebo bílkovin s následující sublimací vody patří ke konzervačním postupům. Lyofilizované kultury mají životnost několik let. Také ve zmrazených potravinách, které se skladují při teplotách –15 až –18 °C, přežívá většina bakterií po dobu delší než rok. Zmrazením potravin dochází jen k zastavení činnosti mikroorganismů, ale ne k jejich usmrcení. K procesům mrazení jsou odolnější grampozitivní bakterie než gramnegativní. Po rozmrazení se potraviny rychleji kazí [1].
Působení vysokých teplot
Teplota, která má smrtící účinek na mikroorganismy, je označována jako teplota letální. Je to nejnižší teplota, při které dochází za určitý čas k usmrcení mikroorganismů. Obecně je to teplota 70 °C působící po dobu 10 minut [1].
Vlivem působení vysokých teplot dochází v buňkách mikroorganismů k denaturaci bílkovin, inaktivaci enzymů a toxinů, k narušení struktur nukleových kyselin a cytoplazmatické membrány. Smrtící účinek vysokých teplot je závislý na druhu a fyziologickém stavu mikroorganismu. Dále pak na charakteru prostředí a koncentraci buněk v prostředí. Jednotlivé druhy mikroorganismů se liší svou termorezistencí, tedy stupněm odolnosti k vysokým teplotám.
Souhrn
Odolnost k vysokým teplotám je závislá:
- na fyziologickém stavu buněk a jejich genetické výbavě,
- na množství mikroorganismů v prostředí,
- na obsahu vody a ochranných látek v prostředí (lipidy, bílkoviny, sacharidy).
Příklad
V praxi se smrtících účinků vysokých teplot využívá velmi často. Například ke sterilizaci různých předmětů, živných půd pro pěstování mikroorganismů a ke konzervaci potravin. Někdy jen ke snížení mikrobiální kontaminace.
Tabulka 2. Tepelné záhřevy
Sterilizace | inaktivace absolutně všech vegetativních forem mikroorganismů i mikrobiálních spor (absolutní sterilita) |
Sterilace | inaktivace vegetativních forem mikroorganismů i mikrobiálních spor nežádoucích mikroorganismů (obchodní sterilita) |
Pasterizace | inaktivace všech vegetativních forem mikroorganismů |
Pasterace | inaktivace vegetativních forem nežádoucích mikroorganismů |
Tyndalace | opakovaná (frakcionovaná) pasterace a inaktivace přítomných bakteriálních spor po jejich vyklíčení |
Blanšírování | inaktivace enzymů a snížení mikrobiální kontaminace |
+
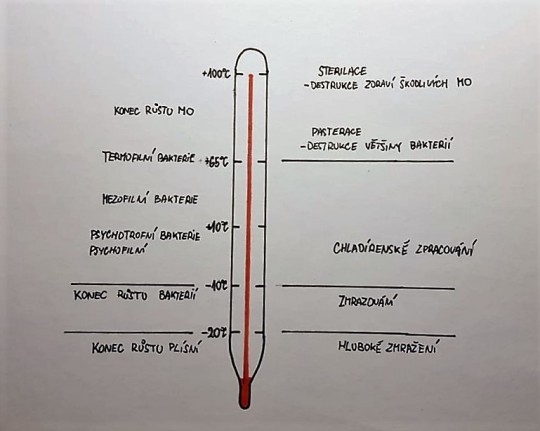
Obr. 3. Růst mikroorganismů při různých teplotách
1.3.2.2
Relativní vlhkost vzduchu
Zjednodušeně jde o obsah vody ve vzduchu. Když je relativní vlhkost vzduchu vysoká, ovlivňuje vodní aktivitu potraviny. Čím vyšší je teplota, tím nižší musí být relativní vlhkost prostředí a naopak, aby se údržnost potraviny zvýšila.
Poznámka
Potraviny, které mají vodní aktivitu pod 0,60, musíme skladovat v prostředí s takovou relativní vlhkostí, která nedovolí zvýšení vlhkosti výrobku. Tím ani vodní aktivita nedosáhne takové výše, aby mohlo dojít k pomnožení mikroorganismů.
+

Obr. 4. Vliv relativní vlhkosti
1.3.2.3
Složení atmosféry v obalu a skladovacím prostoru
Skladování potravin v řízené atmosféře plynů má u potravin ochranný účinek. U vakuově balených potravin v obalech nepropustných pro kyslík se inhibuje růst aerobních mikroorganismů (např. rod Pseudomonas, některé druhy rodu Bacillus, plísně). Bez přístupu kyslíku dobře rostou anaerobní a mikroaerofilní mikroorganismy. Přítomnost plynů v prostředí obklopujícím potravinu určuje dominantní typ mikroorganismů [2].
Příklad
Využívá se toho při skladování potravin v řízené atmosféře. Používá se CO2, který brání růstu aerobních mikroorganismů – plísní, kvasinek a některých bakterií. Využívá se toho zejména při skladování ovoce a zeleniny. Tento způsob není vhodný u potravin s vysokým obsahem tuku, protože má silné oxidační účinky a způsobuje žluknutí tuků [2].
+
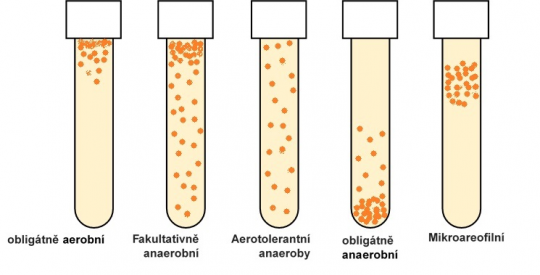
Obr. 5. Rozdělení mikroorganismů ve vztahu ke kyslíku
Tabulka 3. Potravinářsky významné mikroorganismy a jejich nároky na kyslík
Aerobní | Listeria monocytogenes, rod Bacillus, rod Pseudomonas |
Fakultativně anaerobní | Salmonella, Yersinia enterocolitica a ostatní enterobakterie, většina bakterií mléčného kvašení, Staphylococcus aureus |
Anaerobní | rod Clostridium, Bifidobacterium |
1.3.2.4
Čas
Definice
Mezi vnější faktory patří také čas. Platí, že čím je delší doba působení daných faktorů na mikroorganismy, tím efektivnější je jejich účinek.
Vliv jednotlivých faktorů na růst nemůže být posuzován bez vztahu k času. Hlavně při hodnocení vlivu teploty je důležité zvažovat také dobu, po kterou je mikroorganismus teplotě vystaven To platí při úvahách o rychlosti růstu, ale také při posuzování vlivu záhřevu na inaktivaci mikroorganismů. Čím je kratší doba skladování potravin a kratší doba prodlev při jejich výrobě a úpravě, tím je nižší případná kontaminace.
Příklad
Při ideálních podmínkách může mnoho mikroorganismů za každých 15 až 20 minut zdvojnásobit svůj počet. Například ze 100 bakterií může takto vzniknout za jednu hodinu 800 bakterií, za dvě hodiny 6 400, za tři hodiny 51 200, za čtyři hodiny 490 600, za pět hodin 3 276 800. Obdobně se chovají mikroorganismy způsobující onemocnění. Pokud by například v 25 gramech masa bylo přítomno 10 salmonel, bylo by jich po dvaceti minutách již 20, po čtyřiceti minutách již 80 a po jedné hodině již 160.
1.3.3
Vnitřní faktory
1.3.3.1
Složení potravin
Potraviny, které obsahují více nízkomolekulárních látek a větší množství vody, se kazí rychleji. Je to proto, že nízkomolekulární látky mohou mikroorganismy vstřebávat přímo bez předchozího štěpení. Bílkoviny a složené sacharidy (škrob, pektin, celulóza) musí být nejprve mikrobiálními exoenzymy rozštěpeny a pak jsou teprve vstřebávány endoenzymy. Štěpení bílkovin extracelulárními proteázami nastupuje až poté, co jsou spotřebovány snáze dostupné nízkomolekulární složky.
Příklad
Extracelulární enzymy produkují zejména bakterie rodu Bacillus, Clostridium, Pseudomonas, Streptococcus, Lactococcus, Enterococcus a některé druhy čeledi Enterobacteriaceae (např. Proteus). Hnilobné produkty jako sirovodík, amoniak, aminy a organické kyseliny nepříznivě ovlivňují senzorické vlastnosti potravin. Jako zdroj energie využívají mikroorganismy v potravinách cukry, alkoholy, aminokyseliny. Jen málo mikroorganismů je schopno štěpit komplexní sacharidy, jako jsou škrob a celulóza, na jednoduché cukry. Tuky jsou jako zdroj energie využívány jen velmi malým počtem mikroorganismů.
1.3.3.2
Vodní aktivita
Mikroorganismy potřebují pro svůj metabolizmus vodu. Voda se v potravinách vyskytuje ve formě volné, nebo je různými způsoby vázána na složky potravin. Obsah vody v jednotlivých potravinách je značně rozdílný. Souvisí s chemickým složením surovin, ze kterých se potravina skládá, dále se způsobem zpracování a skladování. Nejčastěji se pohybuje mezi 50–90 %. Dle obsahu vody se potraviny rozdělují na potraviny s vysokým, středním a nízkým obsahem.
Příklad
Potraviny obsahující vodu nebo potraviny uložené ve vlhku podléhají biochemickým změnám snadněji než potraviny uložené v suchu. Požadavek vlhkosti odpovídá skladované potravině, vnitřní vlhkost by měla být vždy v rovnováze s vnější vlhkostí. Velká skladovací vlhkost vede ke zvětšení vlhkosti zboží a k urychlení nežádoucích procesů měnících barvu, chuť, vůni a konzistenci, popřípadě i mikrobiologickou jakost výrobku.
Definice
Vodní aktivita (aw) je definována jako poměr parciálního tlaku vodních par nad potravinou k parciálnímu tlaku vodní páry nad destilovanou vodou při určité teplotě [1].
Optimální hodnota aw je pro většinu mikroorganismů > 0,91. Aktivita vody má vliv na neenzymatické hnědnutí potravin, oxidaci lipidů a degradaci ve vodě rozpustných vitamínů, dále pak na enzymatické reakce v potravině a denaturaci proteinů. Hodnota aw také ovlivňuje texturní vlastnosti potraviny [1].
Poznámka
Aktivitu vody lze v potravinách snížit nejen přidáním látek jako jsou cukr, sůl, bílkoviny nebo zvýšením obsahu tuku, ale především se využívají technologické procesy zajišťující odstranění využitelné vody z potravin (sušení, uzení, odpaření, mražení). Při snížení této hodnoty prostřednictvím sušení, uzení, mrazení nebo přídavkem soli či cukru, dojde k výraznému snížení množství vody. Důsledkem této činnosti se zpomaluje růst mikroorganismů [1].
Příklad
Mezi náročné bakterie využívající hodně vody v potravinách patří rod Pseudomonas. Vyskytují se v mléku, vejcích a v mase. Nejvíce odolné vůči nízké hladině aw jsou plísně, méně odolné jsou kvasinky, ještě méně grampozitivní bakterie a nejmenší odolnost se vyskytuje u gramnegativních bakterií.
Většina bakterií způsobujících kažení potravin neroste pod hranicí aw = 0,91, na rozdíl od plísní, které se mohou množit často i pod hranicí aw = 0,80. Převážná část mikroorganismů není schopna růstu při aw pod 0,60. Minimální hodnota aw růstu ovšem není totožná s minimální hodnotou pro tvorbu toxinů [1].
Tabulka 4. Rozsah hodnot vodní aktivity pro růst mikroorganismů.
Vodní aktivita | Inhibice růstu mikroorganismů při dosažení spodní hodnoty vodní aktivity | Příklad potravin |
1,00 – 0,95 | G- tyčinky, většina bakteriálních spor, některé plísně | mléčné výrobky, měkké masné výrobky, ovoce |
0,95 – 0,91 | většina koků, lactobacily, Listeria monocytogenes, vegetativní buňky, čeleď Bacillaceae, některé plísně | syrové šunky, uzené ryby, uzená masa, sýry |
0,91 – 0,87 | neosmofilní kvasinky | trvanlivé salámy, tvrdé sýry |
0,87 – 0,80 | nexerofilní plísně, Staphylococcus aureus | rýže, mouka, slazené kondenzované mléko |
0,80 – 0,75 | většina halofilních bakterií, osmotolerantní kvasinky | cukrovinky, džemy |
0,75 – 0,65 | xerofilní plísně (suché prostředí) | ořechy, parmezán, vyzrálé sýry |
0,65 – 0,60 | osmofilní kvasinky | sušené ovoce, med |
Pod 0,50 | – | těstoviny, koření, sušené výrobky |
Příklad
Většina bakterií je schopna se rozmnožovat v živných prostředích o aw v rozmezí 0,99 – 0,93. Výjimku tvoří některé halotolerantní koky (např. rody Micrococcus, Staphylococcus), které jsou schopny se rozmnožovat i při 10% koncentraci NaCl. Dále existují některé bakterie, které se rozmnožují pouze při nízkých aktivitách vody v prostředí s vysokou koncentrací NaCl (15 % a více). Jedná se o halofilní bakterie. Jejich rozmnožování se naopak zastavuje při nižších koncentracích NaCl (6–10 %) [1].
Minimální hodnota aw kvasinek (0,94 – 0,88) je nižší než u většiny bakterií. Osmotolerantní kvasinky jsou schopny rozmnožování při vodní aktivitě 0,73, která je např. v medu nebo 60% roztoku sacharózy. Tyto kvasinky mohou způsobovat nežádoucí kvašení medu. Osmofilní druhy kvasinek rostou při hodnotách aw 0,65 – 0,61 [1].
Plísně se většinou rozmnožují za nižší vodní aktivity než většina bakterií a kvasinek, výjimkou jsou tzv. vodní plísně. Na druhé straně jsou známé také xerofilní plísně (vyžadují suché prostředí) s dolní hranicí aw 0,60 [1].
Tabulka 5. Vodní aktivita vybraných potravin
Vodní aktivita | Potravina | Činnost mikroorganismů |
0,1 – 0,2 | cereálie, cukr, sůl, sušené mléko | Přežívají, nerozmnožují se, nerostou, počet klesá. |
méně než 0,60 | med, čokoláda, sušenky | Přežívají, nerozmnožují se, nerostou. |
0,60 – 0,85 | džemy, sušené ovoce a zelenina, slané ryby, ořechy, sušené vaječné směsi | Přežívají, plísně při vodní aktivitě pod 0,80 netvoří toxiny. |
0,85 – 0,93 | slanina, fermentované salámy, sušené maso, syrová šunka | Staphylococcus aureus se rozmnožuje, netvoří toxiny. Plísně se rozmnožují a tvoří toxiny. |
0,93 – 0,98 | sýry, kondenzované mléko, rajský protlak, pečivo, ovocné šťávy, tepelně opracované uzeniny | Staphylococcus aureus se rozmnožuje a tvoří toxiny. Bakterie, kvasinky se rozmnožují pomaleji a některé ukončují svůj růst. |
0,98 – 0,99 | vejce, mléko, kompoty, maso, ryby, zelenina v konzervách | Rozmnožují se a rostou. |
Souhrn
Vodní aktivita vyjadřuje množství volné vody využitelné pro mikroorganismy, závisí na druhu potraviny a není shodná s celkovým obsahem vody: Např. ovoce s 80 % vody a mouka s 20 % vody mají stejnou hodnotu aw.
Hodnota aw nezbytná pro růst: [1].
- bakterie > 0,91
- kvasinky > 0,87
- plísně > 0,7
1.3.3.3
pH prostředí
Růst mikroorganismů je také významně ovlivněn koncentrací vodíkových iontů v prostředí. Většina bakterií roste v neutrálním nebo slabě alkalickém prostředí. Pro kvasinky je optimální kyselé prostředí (pH 4,8 – 5,5). Optimální pH pro většinu plísní je poblíž neutrálních hodnot, ale obecně se plísně rozmnožují ve velmi širokém rozmezí pH, tj. od 1,2 až po 11,0.
V níže uvedené tabulce jsou uvedeny hodnoty minima a maxima pH. Je ovšem důležité si uvědomit, že nejde o striktně daná čísla, protože přežívání mikroorganismů je dále závislé i na jiných faktorech než na hodnotě pH.
Tabulka 6. Minimální a maximální hodnoty pH pro přežívání mikroorganismů
Mikroorganismus | Minimální hodnota pH | Maximální hodnota pH |
Escherichia coli | 4,4 | 6,0 – 8,0 |
Bacillus cereus | 4,9 | 9,3 |
Listeria monocytogenes | 4,5 | 9,0 |
Clostridium botulinum typ A, B | 4,5 | 8,5 |
Staphylococcus aureus | 4,0 | 9,8 |
Saccharomyces cerevisiae | 2,3 | 8,6 |
Aspergillus niger | 1,2 | 11,0 |
V mnoha případech mikroorganismy samy ovlivňují pH prostředí pomocí svého metabolismu, např. kyselinotvorné bakterie, plísně a kvasinky snižují pH prostředí. Při hodnotách pH vzdálených od optima klesá odolnost mikroorganismů k teplotě.
Definice
Faktor pH nabývá hodnot od 0 do 14 a je definován jako záporně vzatý dekadický logaritmus koncentrace oxoniových kationtů: pH = –log [H3O+]. Neutrální pH se pohybuje kolem hodnot 7, „kyselejší“ potraviny mají hodnoty nižší, „zásaditější“ naopak vyšší [1].
Kyselost potraviny je významným faktorem, který ovlivňuje růst mikroorganismů a jejich odolnost k působení dalších vlivů, zejména k záhřevu. Mírou kyselosti není chuť, ale koncentrace vodíkových iontů, tedy hodnota pH [1].
Příklad
Dle hodnoty pH se potraviny dělí na kyselé – pH pod 4 a málo kyselé – pH nad 4. Mikroorganismy se z pravidla mohou množit pouze v oblasti mezi pH 4,5 až 8,0. Bakterie většinou lépe rostou v rozmezí hodnoty pH od 5,0 do přibližně 7,0; plísně a kvasinky mají rozsah hodnot širší. Mezi mikroorganismy existují také výjimky (např. bakterie mléčného kvašení, kvasinky a plísně) jež jsou schopny se rozmnožovat i při hodnotách pH 3,0 a méně, nebo naopak až 9,0. Naproti tomu hnilobné bakterie jsou velmi citlivé k nízkému pH, čehož se využívá při konzervaci potravin (marinované ryby, zelenina v kyselém nálevu nebo mléčně zkvašená zelenina). Minimální hodnota pH pro většinu bakterií, které se podílí na kažení potravin, je 4,4 – 4,6 [1].
Kvasinky vyžadují pro růst kyselé prostředí (optimum pH 4,8 – 5,5) a již slabě alkalické prostředí jejich růst zastavuje. Optimální pH většiny plísní je poblíž neutrálního bodu, avšak mohou se rozmnožovat ve velmi širokém rozmezí pH (1,2 – 11,0). Při silně kyselém pH prostředí (do 2,0) se rozmnožují druhy tvořící značné množství organických kyselin (např. někteří zástupci rodu Penicillium či Aspergillus) [1].
Tabulka 7. Příklady pH vybraných potravin
Interval pH | Potravina | Hodnota pH |
alkalické pH > 7,0 | vaječný bílek | až 9,6 |
neutrální pH 7,0 – 6,5 | mléko povrch sýrů zrajících pod mazem ústřice | 6,7 – 6,5 7,0 – 6,8 6,7 – 6,3 |
slabě kyselé pH 6,5 – 5,3 | ryby zralé sýry maso bílý chléb | 6,6 – 5,7 5,9 – 5,5 5,8 – 5,4 6,0 – 5,0 |
středně kyselé pH 5,3 – 4,5 | konzervy | 5,3 – 4,7 |
kyselé pH 4,5 – 3,7 | kysaná zelenina kyselá mléka, jogurty majonézy | 4,5 – 3,5 4,2 – 3,8 4,1 – 3,0 |
velmi kyselé pH < 3,7 | jablka švestky citróny | 3,5 – 3,3 3,0 – 2,8 2,4 – 2,2 |
Souhrn
Mezní hodnota pH 4,0 (hranice pod kterou neklíčí spory sporulující bakterie Bacillus coagulans)
- potraviny kyselé pH < 4
- potraviny málo kyselé pH > 4
1.3.3.4
Redox potenciál
Dalším vnitřním faktorem v potravinách, který má vliv na růst a metabolismus mikroorganismů, je redox potenciál neboli hodnota Eh. Každé prostředí vykazuje určitý oxidačně redukční potenciál, který je dán přítomností oxidačních nebo redukčních činidel [1].
- oxidační činidla – kyslík, dusičnany, peroxidy
- redukční činidla – vodík, železité ionty, sloučeniny s reaktivními dvojnými vazbami
Definice
Oxidačně redukční potenciál prostředí je rozdíl potenciálu mezi platinovou (kovovou) elektrodou umístěnou do daného prostředí a standardní vodíkovou elektrodou. Oxidační proces je definován odevzdáváním elektronů, redukční proces jejich přijímáním [1].
V prostředí, ve kterém se vyskytují oxidační a redukční látky, vzniká určité napětí tzv. oxidačně-redukční potenciál. Mikroorganismy se značně liší svým vztahem ke kyslíku, a proto také vyžadují různý oxidačně redukční potenciál. Růst aerobních mikroorganismů závisí na přítomnosti rozpuštěného kyslíku, a tedy na pozitivním oxidačně redukčním potenciálu. Fakultativně anaerobní bakterie tolerují pozitivní i negativní oxidačně redukční potenciál. Anaerobní mikroorganismy působení kyslíku a pozitivní oxidačně redukční potenciál nesnášejí a v některých případech je zabíjí (vyžadují tedy negativní oxidačně redukční potenciál).
Příklad
Pro srovnání: Aerobní bakterie rostou při pozitivních hodnotách oxidačně redukčního potenciálu v rozmezí +200 až +400 mV při pH 7. Obligátně anaerobní bakterie začínají růst při hodnotách –200 až –250 mV, kdy konečný potenciál může být až –400 mV.
Poznámka
Oxidačně redukční potenciál je závislý na poměru oxidovaných a redukovaných látek. Obsah těchto látek v potravinách je určený chemickým složením dané potraviny a parciálním tlakem kyslíku v ní. Přidáním redukujících látek, jako je kyselina askorbová, růstem aerobních nebo naopak anaerobních mikroorganismů, dále vakuovým balením atd. dochází ke snížení oxidačně redukčního potenciálu.
Příklad
V potravinářství se toho využívá při balení výrobků do vakuových obalů nebo do obalů s různým složením plynů, čímž se prodlužuje trvanlivost potravin. V potravinách skladovaných v jiné atmosféře než je vzduch, se mikroorganismům, které potřebují k růstu kyslík, životní podmínky ztíží. Balené potraviny můžeme vakuovat a do vakuového balení se mohou dodatečně přidat ochranné plyny jako je třeba dusík, oxid uhličitý nebo oxidy dusíku. Takto můžeme zabránit rozvoji jen určité skupině mikroorganismů. Vakuové balení nelze pokládat za dokonalý konzervační zákrok. Naopak vytvoříme podmínky pro rozvoj anaerobních mikroorganismů (nebezpečným zástupcem je Clostridium botulinum). Proto je třeba dodržovat souhrn více konzervačních zákroků současně (vakuové balení, chlazení, marinace atd.).
1.3.3.5
Textura
Některé potraviny chrání před kontaminací mikroorganismy přirozené krytí povrchu. Například skořápka vajec nebo ořechů, kůže na povrchu ryb a masa, vazivová pouzdra orgánů a povázky masa, kůrka na povrchu pečiva, slupky na ovoci apod.
1.3.3.6
Obsah přirozených antimikrobiálních látek
Definice
Antimikrobiálními látkami rozumíme takové látky, které jsou schopny inhibovat růst mikroorganismů.
V poslední době dochází k rostoucímu zájmu o využívání přírodních antimikrobiálních látek. Mezi ně patří látky antibakteriální, antimykotické, antiparazitické, antiseptické nebo antivirové. Tyto přírodní látky mohou působit na mikroorganismus různými účinky. Mohou být využity např. v potravinářství, farmakologii, kosmetice.
Poznámka
Mechanismus účinku antimikrobiálních látek je velmi složitý a nebyl dosud zcela objasněn. Některé látky mohou působit současně i několika mechanismy. Mechanismy působení mohou vzájemně souviset se složením buněčné stěny a cytoplasmatické membrány mikroorganismu, dále mohou záviset např. na typu mikroorganismu.
Příklad
Některé druhy rostlin obsahují přirozeně se vyskytující éterické oleje, které brání napadení patologickými mikroorganismy. Například hřebíček obsahuje eugenol, česnek allicin a v oregánu se vyskytuje thymol. Samozřejmě i živočišné potraviny vykazují antimikrobiální aktivitu. Nejznámější potravinou je kravské mléko, které obsahuje laktoferin, konglutinin a laktoperoxidázový systém. Další potravinou jsou vejce obsahující lysozym a ovotransferin, který inhibuje Sallmonelu enteritidis. Ovoce a zelenina obsahují deriváty kyseliny hydroxyskořicové. Zelí, kapusta a brokolice obsahují glukosinoláty, které se vyplaví při rozrušení buněk. Vyplavený isothiokyanát pak vykazuje antibakteriální aktivitu.
1.3.4
Další faktory
1.3.4.1
Mechanické vlivy
Jde o druhy poškození, kdy je narušen přirozený tvar a struktura suroviny.
Příklad
Je to například poškození živočišnými škůdci, pomačkání a otlučení ovoce při sběru, dovozu a nakonec i při vlastním zpracování. Taktéž při bourání masa dochází ke změnám struktur ovlivňujících údržnost potravin.
Mechanickým vlivům se lze vyhnout opatrností při manipulaci.
1.3.4.2
Tlak
Mikroorganismy se většinou rozmnožují za normálního atmosférického tlaku. Zvýšením tlaku na 10 až 20 MPa se obyčejně rozmnožování mikroorganismů zpomaluje a při tlaku 30 až 40 MPa se rozmnožování většiny mikroorganismů zcela zastaví. Citlivější je dělení buněk než růst biomasy, takže při určitých tlacích rostou bakterie ve formě vláken [1].
Zajímavost
Některé bakterie v přírodě se dokázaly přizpůsobit vysokému hydrostatickému tlaku, jako např. barofilní nebo barotolerantní bakterie a archea, které byly nalezené v oceánech v hloubce více než 7 000 m.
Předpokládá se, že vysoký tlak působí nepříznivě především na syntézu buněčné stěny. Pro usmrcení mikroorganismů je zapotřebí tlaku kolem 600 až 700 MPa. Doba jeho působení je uváděna v rozmezí několika minut až hodin. Spory jsou odolnější k působení vysokého tlaku [1].
1.3.4.3
Povrchové napětí
Povrchové napětí kapalin vede spolu se špatnou smáčitelností některých mikroorganismů k tomu, že tyto mikroorganismy rostou ve formě blanky (křísu) nebo vláknité vrstvy na povrchu kapalných půd. Sníží-li se povrchové napětí kultivačního prostředí přídavkem povrchově aktivních látek (tenzidů, surfaktantů), rostou tyto mikroorganismy v kapalině submerzní formou, neboť tenzidy současně zvýšily smáčitelnost buněk [1].
Definice
Povrchově aktivní látky jsou sloučeniny obsahující hydrofobní část a hydrofilní část molekuly. Tyto sloučeniny se hromadí na rozhraní dvou fází a také na povrchu buněk mikroorganismů v kapalném prostředí [1].
Přispívají k lepšímu rozptýlení buněk, především u druhů tvořících shluky buněk, a zlepšují jak příjem živin buňkou, tak i exkreci produktů metabolismu. Proto se jimi zrychluje růst některých velmi pomalu se rozmnožujících mikroorganismů (rody Mycobacterium a Propionibacterium). Z povrchově aktivních látek jsou k tomuto účelu nejvhodnější neionogenní tenzidy (např. Tween 80) [1].
Podle hydrofobní části rozlišujeme anionaktivní tenzidy (mýdla) a kationaktivní tenzidy (invertní mýdla). Anionaktivní tenzidy ve vyšších koncentracích poškozují cytoplazmatickou membránu a tím usmrcují buňky. Vyšší koncentrace mohou denaturovat i bílkoviny. Anionaktivní tenzidy, především alkylsulfáty a alkylsulfonáty, jsou také intenzivní smáčedla, a proto zvyšují účinnost roztoků dezinfekčních prostředků. Kationaktivní tenzidy mají už ve velmi nízkých koncentracích, které ještě nevedou k poškození cytoplazmatické membrány, silné mikrobicidní účinky. Jejich smáčecí účinnost je však poměrně malá. Nejčastěji se používají kvarterní amoniové nebo pyridiniové soli [1].
1.3.4.4
Záření
Souhrn
Záření přichází na zemský povrch ze Slunce a ostatních mimozemských zdrojů a rovněž vzniká na Zemi z různých umělých zdrojů. Záření mají různou vlnovou délku a energii, čím kratší je vlnová délka, tím vyšší má energii. Rentgenové záření (paprsky X) a γ-záření patří mezi ionizující záření. Toto záření ionizuje vodu a vytváří vysoce aktivní volné radikály, které mají destruktivní účinek na DNA. Účinek záření je závislý na stáří buněk, složení média a teplotě.
Ultrafialové (UV) záření je záření vlnové délky 240 – 300 nm a má silné mutagenní a letální účinky na mikroorganismy. Nejúčinnější je UV světlo o vlnové délce 265 nm, které poškozuje DNA tvorbou pyrimidinových dimerů. UV světlo vyvolává tvorbu toxických peroxidů a ozónu.
Příklad
Vyšší dávky buňky usmrcují (letální účinek), při nižších dávkách buňky přežívají, zvyšuje se však počet mutací. Normální sklo UV záření pohlcuje a chrání tak mikroorganismy před jeho účinky. Přítomnost karotenoidních barviv v buňkách některých kvasinek, bakterií a na povrchu plísňových spor zvyšuje odolnost těchto mikroorganismů k UV světlu, zvlášť proti UV složce slunečního záření. Toto záření se používá pouze ke sterilizaci vzduchu, povrchovou sterilizaci předmětů, pracovních ploch, provozního zařízení apod.
Elektromagnetické záření, je-li absorbované buňkou, vyvolává v ní chemické změny – je zdrojem energie pro fotosyntézu, vyvolává orientovanou odpověď (fototropický a fototaktický efekt). Vlnění různých vlnových délek se značně liší svým fyziologickým účinkem na mikroorganismy. Vlnění nejdelších vlnových délek, tj. infračervené záření a Hertzovy vlny (radiové vlny), nemají pravděpodobně letální účinek na mikroorganismy a působí pouze svými tepelnými účinky. Viditelné světlo (380 až 760 nm) má nízký mikrobicidní účinek a slouží především jako zdroj energie pro fototrofní mikroorganismy [1].
Příklad
Nejvíce světla pro svůj růst vyžadují plísně. Většina nefotosyntetizujících mikroorganismů světlo nepotřebuje, dokonce některé z nich může poškozovat. Všeobecně bakterie rostou nejlépe ve tmě, proto se v laboratoři kultivují bez přístupu světla v uzavřených termostatech. Přístupem světla je v některých případech podpořena tvorba karotenoidních barviv kvasinek a bakterií.
Přímé sluneční záření působí na mikroorganismy destruktivně tehdy, pokud nemají přirozenou ochranu, např. sliz nebo pigmenty. Toxicky může působit i samotné viditelné světlo při delší expozici, zejména modré a modrofialové spektrum. Ionizační záření má silný letální a mutagenní účinek. Nejcitlivější jsou gramnegativní bakterie, kvasinky a plísně jsou odolnější. Spory a vegetativní formy buněk bývají zpravidla stejně odolné. Nejúčinnější je γ-záření [2].
Příklad
V potravinářské praxi se využívá poměrně často pro zajištění bezpečnosti a trvanlivosti koření, dále pak u sušených bylin, zeleniny, luštěnin, rýže, drůbežího masa, ryb a dalších. Jeho použití je ošetřeno legislativou [2].
Záření o vlnové délce kratší než 10 nm (Rentgenovo záření, γ-záření a kosmické záření) mají na mikroorganismy silné mutagenní i letální účinky. Kromě mikrobiálních buněk jsou vysoce škodlivé i pro buňky vyšších organismů. Účinek ionizačních záření je vyvolán přímým působením na citlivé molekuly buňky (např. DNA) a také prostřednictvím volných radikálů a oxiranů, které vznikají v důsledku těchto záření na buňku a její okolí a způsobují tak nespecifickou ionizaci biomolekul a neopravitelnou ztrátu jejich funkce. K ionizujícímu záření jsou velmi citlivé gramnegativní bakterie, zatímco grampozitivní bakterie, kvasinky a plísně jsou odolnější. K dosažení letálního účinku na mikroorganismy je zapotřebí o hodně vyšší dávky, než jaká je smrtící dávka pro člověka. Spory bakterií nejsou k tomuto záření o mnoho odolnější než příslušné vegetativní formy [1].
β-záření má na mikroorganismy podobné účinky jako γ-záření, avšak jeho pronikavost hmotou je mnohem menší.
1.3.4.5
Antibiotika
Definice
Jsou organické sloučeniny produkované mikroorganismy, které mají schopnost v nepatrné koncentraci potlačovat růst jiných mikroorganismů nebo je usmrcovat.
Jako antibiotika jsou označovány látky získané původně jako přírodní produkty mikroorganismů. Jejich účinek je založen na zastavení růstu a rozmnožování nebo na usmrcování mikrobiálních buněk. Antibiotika lze dělit na skupiny dle různých kritérií: podle spektra účinku, typu účinku a mechanismu účinku.
Spektrem účinku antibiotika rozumíme výčet kmenů citlivých k určitému antibiotiku. Rozlišujeme látky s úzkým spektrem účinku, tzv. antibiotika s cíleným účinkem, a rozšířeným nebo širokým spektrem účinku, což jsou antibiotika účinná proti celé řadě různých patogenů, ať už se jedná o G+ nebo G- mikroorganismy. Mezi antibiotika širokospektrá se řadí např. tetracykliny. Jak již bylo zmíněno, antibiotika mohou působit dvěma typy účinků. Prvním z nich je bakteriostatický účinek. Pokud antibiotika působí bakteriostaticky, dojde k zastavení růstu a rozmnožování bakterií. V případě baktericidního účinku antibiotikum způsobí usmrcení bakterií.
Dalším možným dělením antibiotik je dělení dle mechanismu jejich účinku. Zde je třeba zmínit, že bakterie patří do skupiny prokaryotických organismů, obsahují buněčnou stěnu a jejich nukleové kyseliny nalezneme v jádře.
Poznámka
Existují dva typy bakteriální stěny, buněčná stěna G+ bakterií a G- bakterií. V případě G+ bakterií obsahuje buněčná stěna velké množství peptidoglykanů, jejichž tvorbu je možno zastavit právě některými antibiotiky, tím pak dojde k likvidaci buňky. G- bakterie mají pouze tenkou vrstvu peptidoglykanů, ale obsahují povrchovou fosfolipidovou dvouvrstvu a v periplazmatickém prostoru mají nahromaděné beta-laktamázy, které rozkládají řadu antimikrobiálních látek a jsou tak odolnější. Tyto odlišnosti znamenají zásadní rozdíl v odolnosti vůči různým typům antimikrobiálních látek.
+
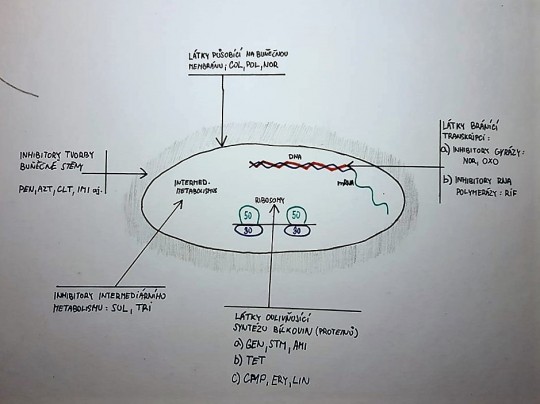
Obr. 6. Možnosti působení antibiotik
1.3.4.6
Elektrický proud
Střídavý elektrický proud o malé intenzitě (30 až 100 mA) nemá nepříznivý vliv na mikroorganismy. Střídavý proud o vyšší intenzitě působí nepříznivě svými tepelnými účinky. Stejnosměrný elektrický proud může mikroorganismy nepříznivě ovlivňovat svými elektrolytickými účinky, kdy mohou v prostředí vznikat mikrobicidní sloučeniny [1].
1.3.4.7
Ultrazvuk
Zvukové vlny o frekvenci vyšší než 20 kHz (ultrazvuk) působí na mikroorganismy letálně tehdy, mají-li poměrně velkou intenzitu a nízký kmitočet. Jedná se o tzv. kavitační ultrazvuk. V důsledku kmitání vzniká prudká pulzace buněčných membrán a cytoplazmy doprovázená rychlým střídáním tlaku. V místech o nízkém tlaku se tvoří trhliny (kavitační bubliny), kam difundují plyny rozpuštěné v kapalině. Při náhlém stlačení těchto bublin vzniká obrovský tlak, který mechanicky porušuje buňky a usmrcuje je [1].
Poznámka
Letální účinek ultrazvuku není 100%, slouží hlavně v laboratorních podmínkách k rozbití mikrobiálních buněk za účelem získání enzymů nebo jiných složek buněčné hmoty. K účinkům ultrazvuku jsou nejcitlivější tyčinkovité a vláknité mikroorganismy, koky a kvasinky jsou poměrně odolné. Nekavitační ultrazvuk, tj. ultrazvuk o velmi vysoké frekvenci a nízkém kmitočtu, nemá nepříznivý vliv na biologický materiál a používá se k lékařským diagnostickým účelům [2].
1.3.4.8
Dezinfekční látky
K odstranění nežádoucích mikroorganismů z vnějšího prostředí používáme dezinfekční látky – např. k dezinfekci nástrojů nebo rukou. Důležité je, aby dezinfekční látky byly toxické jen pro mikroorganismy, a to už při nízkých koncentracích.
1.3.4.9
Chemoterapeutika
Definice
Jsou to látky s toxickým účinkem na mikroorganismy, ale nepůsobí negativně na vyšší organismy.
Nejzávažnější jsou ta chemoterapeutika, která inhibují syntézu důležitých vitaminů nebo látky, které se inkorporují do molekul bílkovin a nukleových kyselin.
Příklad
Nejstarší chemoterapeutika jsou sulfonamidy s vysokou antibakteriální selektivitou. Sulfonamidy mají široké spektrum antibakteriálního účinku (meningokoky, shigely, stafylokoky, streptokoky, některé gramnegativní bakterie).