7.1
Horizontální metoda stanovení počtu presumptivního Bacillus cereus – Technika počítání kolonií vykultivovaných při 30 °C
Definice
ČSN EN ISO 7932 Mikrobiologie potravin a krmiv – Horizontální metoda stanovení počtu presumptivního Bacillus cereus – Technika počítání kolonií vykultivovaných při 30 °C
Tato norma popisuje horizontální metodu stanovení počtu životaschopných presumptivních bakterií druhu Bacillus cereus, a to technikou počítaní kolonií vykultivovaných při 30 °C. Platí pro výrobky určené pro lidskou výživu a ke krmení zvířat a vzorky z prostředí potravinářských výroben a prodejen.
Stanovení tohoto zdravotně významného podmíněně patogenního druhu je založeno na důkazu lecitinázy na masopeptonovém agaru s vaječným žloutkem. Selektivita a diagnostická hodnota se zvyšuje přídavkem mannitolu, fenolové červeně a polymyxinu B.
Poznámka
Z důvodu proveditelnosti této zkušební metody byl stupeň konfirmace redukován na typické znaky kolonií na MYP agaru a test k průkazu hemolýzy. Označení "presumptivní" bylo zavedeno s cílem vyjádřit skutečnost, že pomocí zde uvedeného stupně konfirmace nelze odlišit B. cereus od blízce příbuzných druhů (např. B. anthracis, B. thuringiensis, B. weihenstephanensis, B. mycoides).
7.1.1
Princip
Na povrch tuhé selektivní kultivační půdy v Petriho miskách se očkuje určený objem zkušebního vzorku, nebo určený objem výchozí suspenze. Jako zkušební půda je stanovena půda MYP (Mannitol Yolk Polymyxine B agar). Stejně se postupuje při očkování desetinásobných ředění zkušebního vzorku nebo výchozí suspenze na další plotny. Inokulované Petriho misky se kultivují v termostatu aerobně při 30 °C po dobu 18 – 48 hodin. Následuje konfirmace vybraných typických kolonií na KA a podle výsledků konfirmace, kdy hodnotíme hemolytickou aktivitu, se provede úprava počtu kolonií na miskách. Počet B. cereus v 1 gramu nebo v 1 mililitru vzorku se vypočítá z počtu konfirmovaných kolonií vyrostlých na plotnách.
+
Obr. 26. Živná půda MYP
+
Obr. 27. Živná půda KA
7.1.2
Postup
Zkoušený vzorek asepticky otevřeme a připravíme příslušný počet ředění, který vychází z předpokládaného počtu mikroorganismů. Očkujeme roztěrem na MYP agar, který je nalitý na plotnách, a to vždy novou sterilní pipetou po 0,1 (0,2) ml souběžně na dvě Petriho misky.
Pokud je u některých výrobků žádoucí stanovit nízký počet B. cereus, pak můžeme zvýšit záchytnost tím, že očkujeme 1 ml inokula na povrch jedné velké Petriho misky o průměru 140 mm nebo rozděleně po 0,33 ml na povrch tří Petriho misek o průměru 90 mm. V obou případech očkujeme paralelně na dvě velké misky nebo šest malých misek.
Inokulum se co nejrychleji pečlivě rozetře po povrchu misky pomocí roztírací tyčinky tak, aby nedošlo k dotyku tyčinky se stěnou misky. V Petriho miskách uzavřených víčkem se inokulum nechá vsáknout do agarové půdy při laboratorní teplotě po dobu asi 15 minut. Naočkované misky obrácené dnem vzhůru se inkubuji 18 – 24 hodin při 30 °C, případně dalších 24 hodin.
7.1.3
Hodnocení
Odečítání výsledků provádíme po 24 hodinách, nejsou-li kolonie zřetelně viditelné, inkubujeme misky dalších 24 hodin. Po ukončení inkubace se vyberou misky, přednostně očkované dvěma po sobě následujícími ředěními, na nichž vyrostlo méně než 150 kolonií. Kolonie presumptivního B. cereus se spočítají na každé z ploten zvlášť.
Pokud na miskách naočkovaných neředěným tekutým výrobkem, nebo naočkovaných nejnižším ředěním u ostatních výrobků, vyrostlo méně než 15 typických kolonií, lze provést odhad počtu. V případě, že jsme použili k očkování inokulum 1 ml rozděleně na 3 misky, pak pro následující počítání a konfirmaci uvažujeme, tak jako by to byla jedna miska.
+
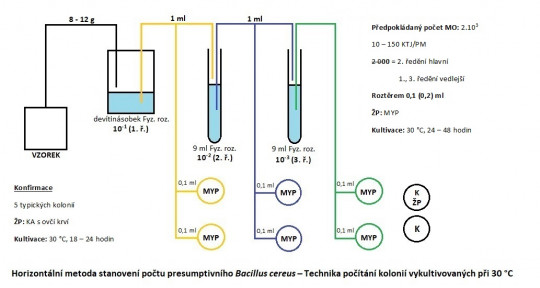
Obr. 28. Schéma rozboru
7.1.4
Morfologie charakteristických kolonií
7.1.4.1
MYP agar
Typické kolonie B. cereus po 24 hodinách kultivace:
- Velké suché drsné kolonie světle růžové barvy (negativní mannitol), s nepravidelnými okraji, obklopeny růžovou zónou precipitace (tvorba lecitinázy).
Atypické kolonie B. cereus po 24 hodinách kultivace:
- Pokud v Petriho miskách došlo k růstu jiných mikroorganismů, které jsou schopné využívat mannitol za tvorby kyseliny, může být typické růžové zbarvení kolonií B. cereus ovlivněno. Nejčastěji dochází k zeslabení nebo vymizení barvy.
- Některé kmeny druhu B. cereus tvoří velice málo lecitinázy, nebo ji nevytvoří vůbec. Tyto kolonie pak nejsou obklopeny zónou precipitace a je nutné podrobit je konfirmačnímu testu.
+
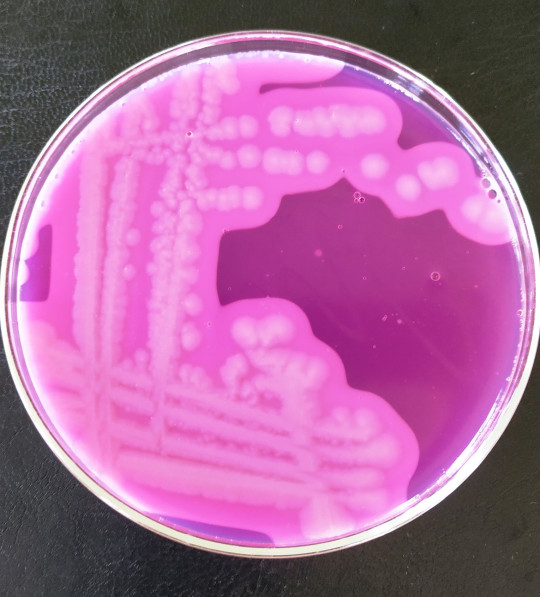
Obr. 29. Typické kolonie B. cereus na MYP
7.1.4.2
KA
Typické kolonie B. cereus po 24 hodinách kultivace:
- Velké suché drsné kolonie s nepravidelnými okraji, šedé až bílé barvy. Kolonie jsou obklopeny různě velkou zónou β-hemolýzy. Dále je indikován typický zápach po myšině.
+
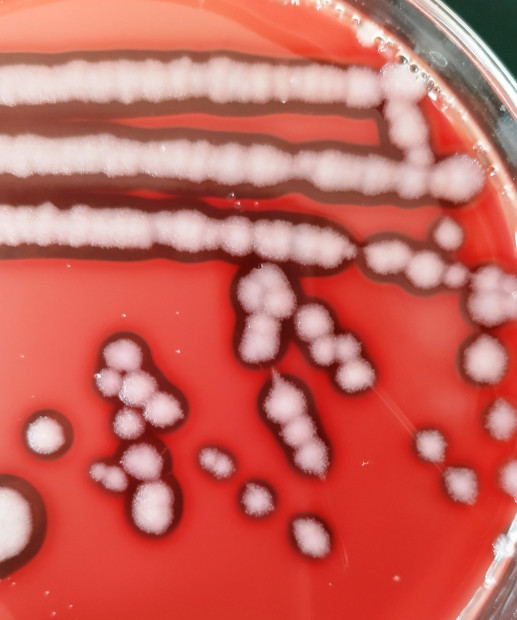
Obr. 30. Typické kolonie B. cereus na KA
7.1.5
Konfirmace
Z každé plotny vybrané k výpočtu se vybere po pěti typických koloniích. Pokud na plotně vyrostlo méně typických kolonií než pět, vyberou se všechny. Pokud se na plotnách vytvořil souvislý nárůst a není možné vybrat kolonie jako dobře izolované, vybere se odtud pět typických kolonií a každá z nich se subkultivuje na plotnu kompletní půdy (MYP agar). Inkubujeme při 30 °C po dobu 18 – 24 hodin. Z každé plotny se vybere nejméně jedna dobře izolovaná růžově zbarvená kolonie. Tato kolonie se konfirmuje.
7.1.5.1
Test k průkazu hemolýzy na agaru s ovčí krví
Část vybrané kolonie se naočkuje na povrch agaru s ovčí krví čarou, vpichem nebo ve formě kapky způsobem, který umožňuje dobrou interpretaci hemolytické reakce. Inkubuje se při 30 °C po dobu 24 hodin a poté se hodnotí hemolytická reakce.
7.1.6
Vyjádření výsledků
Pokud je alespoň 80 % kolonií, které byly z dané misky vybrány ke konfirmaci potvrzeno jako presumptivní B. cereus, počet kolonií na misce se nijak neupravuje. Ve zbylých případech se počet kolonií na misce musí upravit podle procentuálního podílu zastoupených konfirmovaných kolonií z celkového počtu kolonií, které byly vybrány ke konfirmaci (1 kolonie – 20 %, 2 kolonie – 40 %, 3 kolonie – 60 %, 4 kolonie – 80 %, 5 kolonií – 100 %).
Jestliže na dvou miskách naočkovaných neředěným zkušebním vzorkem nebo výchozí suspenzí nebyly zjištěny žádné kolonie presumptivního B. cereus, vyjádří se výsledek takto:
- méně než 1 presumptivní B. cereus v mililitru (pro tekuté výrobky)
- méně než 1/d presumptivní B. cereus v gramu (pro ostatní výrobky), kde d je ředící faktor výchozí suspenze
Příklad
Úkol: Stanovte Bacillus cereus v předloženém vzorku.
Postup:
- Zaznamenejte si do poznámek předpokládané hodnoty výskytu mikroorganismů, vypočítejte příslušný počet ředění, nakreslete a popište schéma rozboru, uveďte všechny důležité informace.
- Připravte si aseptické prostředí a pomůcky, které budete potřebovat, proveďte přípravné práce.
- Otevřete asepticky obal vzorku, upravte vzorek a proveďte navážku (8 – 12 g s technickou přesností) do homogenizačního sáčku nebo prachovnice.
- Vypočtěte množství (devítinásobek) ředícího roztoku (fyziologického roztoku, případně citronanu sodného).
- Homogenizujte, použijte metodu podle povahy vzorku.
- Očkujte roztěrem 0,1 (0,2) ml inokula na Petriho misky s MYP.
- Očkujte hlavní a dvě vedlejší ředění – tři po sobě jdoucí ředění paralelně do dvou Petriho misek dle schématu, současně se očkuje kontrola roztěru.
- Naočkované plotny obrácené dnem vzhůru inkubujte 18 – 24 hodin při 30 °C. Pokud nejsou kolonie zřetelně viditelné, inkubujte ještě dalších 24 hodin.
Hodnocení:
Vytvořte tabulku počtu mikroorganismů na Petriho miskách, proveďte výpočet KTJ podle vhodného vzorce.
Závěr:
Zhodnoťte stanovení, vyjádřete správně množství mikroorganismů ve vzorku. Porovnejte výsledky v celé skupině.