6.2
Stanovení anaerobních sporulujících bakterií
Stanovení je založeno na selekci spor inaktivačním záhřevem nebo chemickými činidly (neomycin, polymyxin, azid sodný) a následnou kultivací za nepřístupu vzduchu nebo na půdách obsahujících redukující látky.
Zjišťovat se mohou všechny anaerobní sporulující bakterie bez bližší diferenciace, nebo se rozlišují fakultativně anaerobní bacily od klostridií, případně některé skupiny a druhy rodu Clostridium (C. perfringens). Používá se k tomu selektivně diagnostických půd umožňujících určit rozdílnou schopnost redukovat sulfity na sulfidy, specificky měnit vzhled půdy s vaječným žloutkem a růst v přítomnosti některých antibiotik.
6.2.1
Kultivace ve vysokém sloupci půdy
Následující tři uvedené zkoušky jsou nejjednodušší a neumožňují rozlišit druhy rodu Clostridium od fakultativně anaerobních druhů rodu Bacillus. Uskutečňují se kultivací ve vysokém sloupci půdy převrstvené sterilní parafin-vazelínovou směsí nebo parafinovým olejem. Množství spor přítomných ve vzorku se zjistí podle počtu pozitivních zkumavek očkovaných řadou za sebou následujících desítkových ředění technikou MPN.
6.2.1.1
Upravený Weinzirlův test
Používá se hlavně ke kontrole mléka. Do sterilního mléka ve zkumavce se napipetuje vzorek. Převrství se 5 – 10 mm vysokou vrstvou sterilní parafin-vazelínovou směsí. Inaktivuje se ve vodní lázni při 85 °C 10 minut. Pak se vychladí na 37 °C a při této teplotě inkubuje 5 dní. Jsou-li sporuláty přítomny, způsobí koagulaci, peptonizaci nebo tvorbu plynu, případně kombinaci uvedených projevů. Počet spor se stanoví technikou MPN.
6.2.1.2
Stanovení v játrovém bujónu
Sterilní bujón ve zkumavkách se naočkuje, převrství parafinem, inaktivuje při 80 °C 15 minut. Přítomnost sporulujících anaerobů se projeví zákalem, vznikem sedimentu, tvorbou plynu, po kultivaci 5 – 7 dní při 37 °C. Počet se stanoví technikou MPN.
6.2.1.3
Stanovení v želatinovém agaru s glukózou
Rozpuštěná půda ve zkumavkách, vytemperovaná na 45 °C, se naočkuje a přelije parafinem. Inaktivuje a kultivuje se jako v předcházející metodě. Odečítají se kolonie vyrostlé ve sloupci půdy. Dojde-li k částečnému ztekucení a zákalu půdy, případně rozrušení sloupce půdy vytvořeným plynem, nelze jednotlivé kolonie rozeznat a samostatně odečítat. V takovém případě se výsledky hodnotí jako při použití tekuté půdy technikou MPN.
6.2.2
Kultivace na agarových plotnách v atmosféře bez kyslíku
Naočkované Petriho misky se ukládají do anaerostatů nebo anaerobních komor, nouzově do exikátorů. V těchto zařízeních lze chemickou reakcí vázat volný kyslík obsažený v atmosféře kultivačního prostoru a nahradit jej jinými plyny. Nebo se vzduch odsaje vývěvou a nahradí směsí dusíku, oxidu uhličitého a vodíku. Za těchto podmínek rostou i přísně anaerobní druhy na povrchu půd v Petriho miskách.
6.2.2.1
Anaerostat s generátorem plynů a katalyzátorem
Anaerostaty jsou nádoby určené pro kultivaci anaerobních a mikroaerofilních mikroorganismů. Můžou být z nerezové oceli, tlustostěnného skla nebo z čirého polykarbonátu, nejčastěji s plastovým víkem a přírubou, se zabudovanými ventily a manometrem pro kontrolu tlaku v nádobě. Příslušenství tvoří také vkládací nerezové stojánky pro Petriho misky. Velikost nádoby se nejčastěji pohybuje od 2 do 6 litrů.
Do anaerostatů se vkládá generátor plynů, který je určen k tvorbě anaerobního prostředí. Obsahuje např. směs hořčíku, kyseliny vinné a uhličitanu sodného. Po zvlhčení určitým objemem vody se začnou uvolňovat plyny – vodík a oxid uhličitý. Přibližné složení atmosféry po aktivaci: 71 % dusíku, 10 % oxidu uhličitého, 19 % vodíku. Generátor je určen pro jedno použití.
Dále se vkládá katalyzátor, kterým je kovové paládium na aluminiovém nosiči. Paládium katalyzuje slučování kyslíku přítomného v nádobě s vyvíjeným vodíkem za vzniku vody. Katalyzátor lze použít opakovaně (až 30x), po každém použití se však musí vysušit v sušárně a uchovávat v exikátoru.
+

Obr. 23. Různé druhy anaerostatů
+
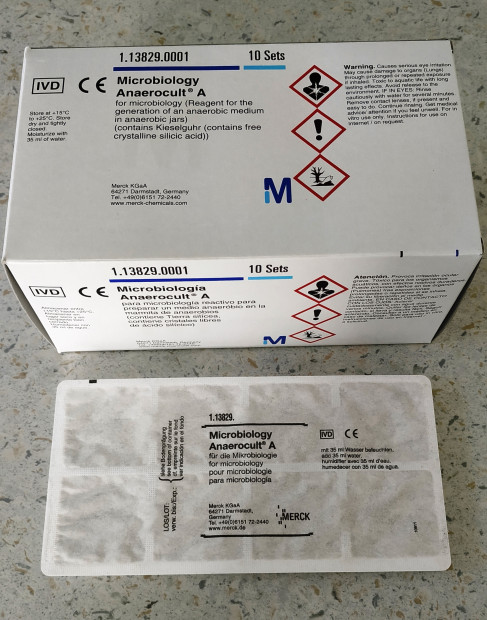
Obr. 24. Generátor plynů
+
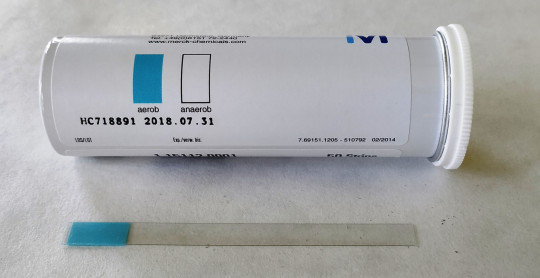
Obr. 25. Indikátor anaerobiózy
Video 1. Uložení do anaerostatu
6.2.3
Kultivace v půdách obsahujících redukující látky
Jestliže živná půda obsahuje sloučeniny snižující dostatečně redox potenciál, mohou anaerobní bakterie růst a tvořit kolonie, i když kultivace probíhá v normální vzdušné atmosféře. Takovými látkami jsou thioglykolát sodný, formaldehyd sulfoxylát sodný, cystin, cystein, kyselina askorbová, redukované železo, extrakty ze srdcí a jater apod. Uvedené principy lze využít jak pro kultivaci v tekutých půdách ve zkumavkách, tak pro kultivaci v agarových půdách v Petriho miskách.
6.2.4
Spolehlivost a přesnost stanovení anaerobních sporulujících bakterií
Výsledky stanovení jsou velmi závislé na použité metodě. Obecně platí, že různé kmeny klostridií nejsou stejně citlivé na záhřev. Pozitivní reakci mohou někdy vyvolat i termorezistentní nesporulující anaerobní bakterie.
Přesnější jsou metody plotnové, které navíc umožňují makroskopickou a mikroskopickou kontrolu kolonií.
Příklad
Úkol: Stanovte anaerobní sporulující bakterie v předloženém vzorku.
Postup:
- Zaznamenejte si do poznámek předpokládané hodnoty výskytu mikroorganismů, vypočítejte příslušný počet ředění, nakreslete a popište schéma rozboru, uveďte všechny důležité informace.
- Připravte si aseptické prostředí a pomůcky, které budete potřebovat, proveďte přípravné práce.
- Otevřete asepticky obal vzorku, upravte vzorek a proveďte navážku (8 – 12 g s technickou přesností) do homogenizačního sáčku nebo prachovnice (podle povahy vzorku).
- Vypočtěte množství (devítinásobek) ředícího roztoku.
- Homogenizujte, metodu zvolte podle povahy vzorku.
- Proveďte inaktivaci tekutého vzorku nebo výchozí suspenze. 10 ml ve zkumavce inaktivujte ve vodní lázni při 85 °C 5 minut.
- Inaktivovanou suspenzi rychle vychlaďte a vytvořte příslušný počet ředění podle předpokládaného počtu mikroorganismů.
- Očkujte přelivem 1 ml inokula. Petriho misky zalijte do 15 minut 15 – 20 ml agarové živné půdy GTK rozvařené a vychlazené na 45 °C, opatrně promíchejte a nechejte ztuhnout, následně dosušte v sušárně při 50 °C 30 minut.
- Očkujte hlavní a dvě vedlejší ředění, tedy tři po sobě jdoucí ředění paralelně do dvou Petriho misek dle schématu, současně se očkuje kontrola živné půdy a kontrola roztěru.
- Petriho misky umístěte dnem vzhůru do anaerostatu a spolu s indikátorem anaerobiózy inkubujte při 30 °C 72 hodin mezofilní anaerobní sporotvorné mikroorganismy.
Hodnocení:
Vytvořte tabulku počtu mikroorganismů na Petriho miskách, proveďte výpočet KTJ podle vhodného vzorce.
Závěr:
Zhodnoťte stanovení, vyjádřete správně množství mikroorganismů ve vzorku, zhodnoťte kvalitu vzorku. Porovnejte výsledky stanovení v rámci celé skupiny.